我国某大城市今年夏季多次降下酸雨。据环保部门测定,该城市整个夏季酸雨的pH平均为3.2。在这种环境中的铁制品极易被腐蚀。对此条件下铁的腐蚀的叙述不正确的是
| A.此腐蚀过程有化学腐蚀也有电化学腐蚀 |
| B.发生电化学腐蚀时的正极反应为2H2O+O2+4e-=4OH- |
| C.在化学腐蚀过程中有氢气产生 |
| D.发生电化学腐蚀时的负极反应为Fe=Fe2++2e- |
汽车等机动车辆的启动电源常用铅蓄电池,放电时的电池反应如下:
PbO2+Pb+2H2SO4=2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
用惰性电极电解下列溶液,一段时间后,停止电解,向溶液中加入一定质量的另一种物质(括号内),能使溶液完全复原的是
| A.CuCl2 (CuO) | B.NaOH (NaOH) |
| C.CuSO4 (CuCO3) | D.NaCl (NaOH) |
一种太阳能电池的工作原理如下图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液,下列说法不正确的是( )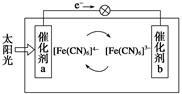
| A.K+移向催化剂b |
| B.催化剂a表面发生的化学反应:[Fe(CN)6]4--e-=[Fe(CN)6]3- |
| C.Fe(CN)63-在催化剂b表面被氧化 |
| D.电解池溶液中的[Fe(CN)6]4-和[Fe(CN)6]3-浓度基本保持不变 |
在下列装置中,MSO4和NSO4是两种常见金属的易溶盐。当K闭合时,SO42-从右到左通过交换膜移向M极,下列分析正确的是( )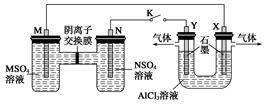
| A.溶液中c(M2+)减小 |
| B.N的电极反应式:N=N2++2e- |
| C.X电极上有H2产生,发生还原反应 |
| D.反应过程中Y电极周围生成白色胶状沉淀 |
用如图所示装置进行实验,下列叙述不正确的是 ( )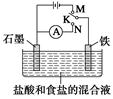
| A.K与N连接时,铁被腐蚀 |
| B.K与N连接时,石墨电极产生气泡 |
| C.K与M连接时,一段时间后溶液的pH增大 |
| D.K与M连接时,石墨电极反应式:4OH--4e-=2H2O+O2↑ |
某小组为研究电化学原理,设计如图装置。下列叙述正确的是( )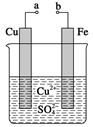
| A.a和b用导线连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为2H++2e-=H2↑ |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极 |
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-=IO+5I-+3H2O,下列说法不正确的是( )
| A.右侧发生的电极反应式:2H2O+2e-=H2↑+2OH- |
| B.电解结束时,右侧溶液中含有IO3— |
C.电解槽内发生反应的总化学方程式:KI+3H2O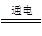 KIO3+3H2↑ KIO3+3H2↑ |
| D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应不变 |
CuI是一种不溶于水的白色固体,它可以由反应: 2Cu2++4I-=2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI-淀粉溶液中阳极周围变蓝色,则下列说法正确的是
| A.若a极变红,则在Pt电极上:2I--2e-=I2淀粉遇碘变蓝 |
| B.若b极变红,在Pt电极上:4OH--4e-=2H2O+O2O2将I-氧化为I2,淀粉遇碘变蓝 |
| C.若a极变红,在Cu电极上:Cu-2e-→Cu2+,2Cu2++4I-=2CuI↓+I2,一段时间后淀粉遇碘变蓝 |
| D.若b极变红,在Cu极上:Cu-2e-═Cu2+,Cu2+显蓝色 |
