题目内容
我国某大城市今年夏季多次降下酸雨。据环保部门测定,该城市整个夏季酸雨的pH平均为3.2。在这种环境中的铁制品极易被腐蚀。对此条件下铁的腐蚀的叙述不正确的是
| A.此腐蚀过程有化学腐蚀也有电化学腐蚀 |
| B.发生电化学腐蚀时的正极反应为2H2O+O2+4e-=4OH- |
| C.在化学腐蚀过程中有氢气产生 |
| D.发生电化学腐蚀时的负极反应为Fe=Fe2++2e- |
B
解析试题分析: B、这种条件下的腐蚀是吸氧腐蚀和析氢腐蚀两种情况都存在,因此错误;
考点:考查金属腐蚀。

练习册系列答案
相关题目
镍氢电池的化学方程式为NiO(OH)+MH Nio+M+H2O(M为储氢合金,电解质
Nio+M+H2O(M为储氢合金,电解质
为KOH),下列说法不正确的是
| A.充电过程中,电池的负极上发生的反应为H2O +M+ e- =MH+OH- |
| B.储氢合金位于电池的负极 |
| C.放电时,OH-离子向电池的负极移动 |
| D.充电过程中,化学能转化为电能储存在电池中 |
某同学按图所示的装置进行电解实验,下列说法错误的是( )。
| A.电解初期,石墨电极上有H2产生 |
| B.整个电解过程中,H+的浓度不断增大 |
| C.电解一定时间后,石墨电极上有铜析出 |
D.电解初期,总反应方程式为: |
下列有关实验的叙述中,合理的是
| A.把SO2通入紫色石蕊试液,可验证SO2的漂白性 |
B.构成如图所示装置时,盐桥中的K+向左池移动 |
| C.配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液浓度偏高 |
| D.将l0 克 ZnSO4·7H2O溶解在90克水中配制10%的ZnSO4溶液 |
下列关于原电池的叙述中正确的是( )。
| A.正极和负极必须是两种不同的金属 |
| B.电子流入的一极为正极 |
| C.原电池工作时,正极和负极上发生的都是氧化还原反应 |
| D.锌、铜和盐酸构成的原电池工作时,锌片上有6.5 g锌溶解,正极上就有0.1 g氢气生成 |
用如图所示装置进行实验,下列叙述不正确的是 ( )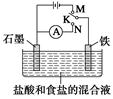
| A.K与N连接时,铁被腐蚀 |
| B.K与N连接时,石墨电极产生气泡 |
| C.K与M连接时,一段时间后溶液的pH增大 |
| D.K与M连接时,石墨电极反应式:4OH--4e-=2H2O+O2↑ |
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法正确的是( )
| A.在熔融电解质中,O2-由负极移向正极 |
| B.通入空气的一极是正极,电极反应为:O2+2H2O+4e-=4OH- |
| C.通入丁烷的一极是负极,电极反应为:C4H10+26e-+13O2-=4CO2+5H2O |
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体为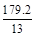 L L |
工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是( )
| A.图1为原电池装置,Cu电极上产生的是O2 |
| B.图2装置中Cu电极上发生的电极反应式为:Cu-2e-=Cu2+ |
| C.由实验现象可知:金属活动性Cu>Cr |
| D.两个装置中,电子均由Cr电极流向Cu电极 |

