甲醇、氧气和强碱溶液做电解质的手机电池中的反应为:
2CH3OH+3O2+4OH-  2CO32-+6H2O,有关说法正确的是
2CO32-+6H2O,有关说法正确的是
| A.放电时,CH3OH参与反应的电极为正极 |
| B.放电时,负极电极反应:CH3OH+8OH--6e- =CO32-+6H2O |
| C.标况下,通入11.2LO2完全反应有1mol电子转移 |
| D.充电时电解质溶液的pH逐渐减小 |
某小组为研究原电池原理,设计如图装置,下列叙述正确的是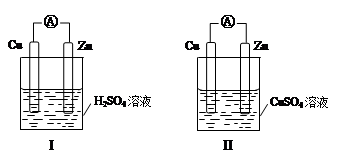
| A.装置I,铜片上有O2逸出 |
| B.装置I,锌片溶解,发生还原反应 |
| C.装置II,电池反应为:Zn+ Cu2+= Zn2++ Cu |
| D.装置II,外电路中,电子从锌电极流向铜电极 |
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是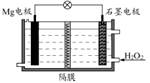
| A.Mg电极是该电池的正极 |
| B.石墨电极附近溶液的pH增大 |
| C.H2O2在石墨电极上发生氧化反应 |
| D.溶液中Cl-向正极移动 |
氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2+ 4OH-- 4e-= 4H2O;O2+ 2H2O + 4e-= 4OH-。据此作出判断,下列说法中错误的是:
| A.H2在负极发生氧化反应 |
| B.供电时的总反应为:2H2+O2=2H2O |
| C.产物为无污染的水,属于环境友好电池 |
| D.燃料电池的能量转化率可达100% |
某原电池的总反应的离子方程式是Zn + Cu2+= Zn2+ + Cu,该原电池的组成正确的是:
| | A | B | C | D |
| 正极 | Zn | Ag | Cu | Cu |
| 负极 | Cu | Cu | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | CuSO4 | FeCl2 |
500 mL KNO3和Cu(NO3)2的混合溶液中c( )=6.0 mol·L-1,用石墨做电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是
)=6.0 mol·L-1,用石墨做电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是
| A.原混合溶液中c(K+)为2 mol·L-1 |
| B.上述电解过程中共转移6 mol电子 |
| C.电解得到的Cu的物质的量为0.5 mol |
| D.电解后溶液中c(H+)为2 mol·L-1 |
某原电池装置如图所示。下列有关叙述中,正确的是( )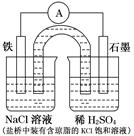
| A.Fe作正极,发生氧化反应 |
| B.负极反应:2H++2e-=H2↑ |
| C.工作一段时间后,两烧杯中溶液pH均不变 |
| D.工作一段时间后,NaCl溶液中c(Cl-)增大 |
番茄汁显酸性,在番茄上平行地插入铜片和锌片形成一个原电池,如图所示。以下叙述正确的是( )
| A.铜片上发生氧化反应 |
| B.锌片为正极,铜片为负极 |
| C.锌片为阴极,铜片为阳极 |
| D.番茄汁起电解质溶液的作用 |
下列金属防腐的措施中,使用外加电流的阴极保护法的是
| A.水中的钢闸门连接电源的负极 |
| B.金属护拦表面涂漆 |
| C.汽车底盘喷涂高分子膜 |
| D.地下钢管连接镁块 |
Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式:2AgCl+ Mg = Mg2++ 2Ag +2Cl-。有关该电池的说法正确的是
| A.Mg为电池的正极 |
| B.负极反应为AgCl+e-=Ag+Cl- |
| C.不能被KCl溶液激活 |
| D.可用于海上应急照明供电 |