题目内容
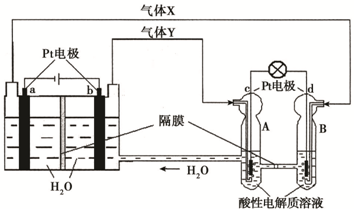
某小组为研究原电池原理,设计如图装置,下列叙述正确的是
| A.装置I,铜片上有O2逸出 |
| B.装置I,锌片溶解,发生还原反应 |
| C.装置II,电池反应为:Zn+ Cu2+= Zn2++ Cu |
| D.装置II,外电路中,电子从锌电极流向铜电极 |
CD
解析试题分析:A、装置I为原电池,铜片上有氢气逸出,错误;B、装置I为原电池,锌片溶解作负极,错误;C、装置II中锌作负极,铜作正极,电池反应为锌与铜离子的置换反应,正确;D、原电池装置中,电子从外电路的负极流向正极,正确,答案选CD。
考点:考查原电池的电极反应、电极判断、电子流向

练习册系列答案
相关题目
如图所示,用铅蓄电池电解100 g 10.0%的硫酸钠溶液,经过一段时间后,测得溶液质量变为95.5 g。下列说法正确的是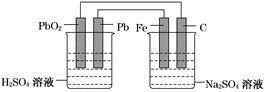
| A.电路中转移0.25 mol电子 |
| B.铅蓄电池中消耗0.5 mol H2SO4 |
| C.铅蓄电池的负极反应式为:PbSO4+2H2O-2e-===PbO2+4H++SO42- |
| D.Fe电极发生的电极反应为Fe-2e-===Fe2+ |
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用右图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。下列说法中,正确的是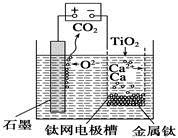
| A.由TiO2制得1 mol金属Ti,理论上外电路转移2 mol电子 |
| B.阳极的电极反应式为C+2O2--4e-=CO2↑ |
| C.在制备金属钛前后,整套装置中CaO的总量减少 |
| D.若用铅蓄电池作该装置的供电电源,“+”接线柱应连接Pb电极 |
某原电池装置如图所示。下列有关叙述中,正确的是( )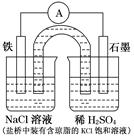
| A.Fe作正极,发生氧化反应 |
| B.负极反应:2H++2e-=H2↑ |
| C.工作一段时间后,两烧杯中溶液pH均不变 |
| D.工作一段时间后,NaCl溶液中c(Cl-)增大 |
下列有关电池的说法不正确的是( )
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气 |
| C.电池反应的化学方程式为CH3CH2OH+O2=CH3COOH+H2O |
| D.正极上发生的反应为O2+4e-+2H2O=4OH- |
21世纪是钛的世纪。在800℃~1 000℃时电解TiO2可制得钛,装置如图所示。下列叙述正确的是( )
| A.a为电源的正极 |
| B.石墨电极上发生还原反应 |
| C.阴极发生的反应为:TiO2+4e-=Ti+2O2- |
| D.每生成0.1 mol钛,转移电子0.2 mol |