下列有关四个电化学装置的叙述正确的是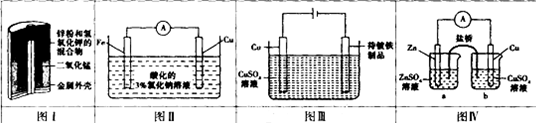
| A.图I装置中MnO2作催化剂 |
| B.图II装置工作一段时间后,滴加少量K3[Fe(CN)6]溶液,无明显现象 |
| C.图III装置中Cu作阳极,为电解液提供Cu2+,保持溶液中Cu2+浓度恒定 |
| D.图IV装置工作时,为平衡电荷,a烧杯中的Zn2+经盐桥移向b烧杯中 |
我国镍氢电池居世界先进水平,我军潜艇将装备国产大功率镍氢动力电池。常见镍氢电池的某极是储氢合金LaNi5H6(LaNi5H6中各元素化合价均可视为零价),电池放电时发生的反应通常表示为LaNi5H6+6NiO(OH)=LaNi5+6Ni(OH)2。下列说法正确的是
| A.放电时储氢合金作正极 |
| B.放电时负极反应为:LaNi5H6-6e-=LaNi5+6H+ |
| C.充电时阳极周围c(OH-)减小 |
| D.充电时储氢合金作负极 |
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是: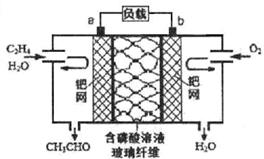
| A.该电池为可充电池 |
| B.每有0.1molO2反应,则迁移0.4mol |
| C.正极反应式为:CH2=CH2-2e-+2OH-=CH3CHO+H2O |
| D.电子移动方向:电极a→磷酸溶液 →电极b |
下列有关电化学的说法正确的是
| A.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 |
| B.电解精炼铜时阴极发生还原反应 |
| C.用铜作电极电解后的硫酸铜溶液中,加入一定量的氧化铜即可恢复溶液的成分和浓度 |
| D.铜锌原电池工作时外电路电子由锌极流向铜极,内电路电子由铜极流向锌极 |
英国赫瑞瓦特大学陶善文博士研究出以尿素为动力的燃 料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,关于该电池描述正确的是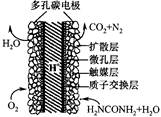
| A.电池工作时H+移向负极 |
| B.该装置还可以将电能转化成为化学能 |
| C.理论上电池工作时,每消耗67.2L O2时,可以净化2mol CO(NH2)2 |
| D.电池的负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+ |
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用。某型甲醇燃料电池的总反应式2CH4O + 3O2 = 2CO2↑+ 4H2O,下图是该燃料电池的示意图。下列说法错误的是( )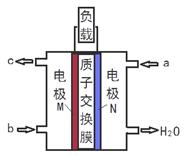
| A.燃料电池将化学能转化为电能 |
| B.a是甲醇、b是氧气 |
| C.质子从M电极区穿过交换膜移向N电极区 |
| D.负极反应:CH4O - 6e- + H2O = CO2↑+ 6H+ |
一种太阳能电池的工作原理示意图如下所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液,下列说法不正确的是( ) 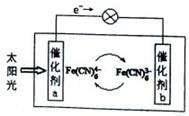
| A.K+移向催化剂b | B.催化剂a表面发生反应:Fe(CN)64――e-=Fe(CN)63- |
| C.Fe(CN)63-在催化剂b表面被氧化 | D.电解质溶液中Fe(CN)63-和Fe(CN)64-浓度基本保持不变 |
通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银)︰n(硝酸亚汞)=2︰1,则下列表述正确的是 ( )
| A.在两个阴极上得到的银和汞的物质的量之比n(银)︰n(汞)=2︰1 |
| B.在两个阳极上得到的产物的物质的量不相等 |
| C.硝酸亚汞的化学式为HgNO3 |
| D.硝酸亚汞的化学式为Hg2(NO3)2 |
某混合溶液中只含有两种溶质NaCl和H2SO4,且n(NaCl)︰n(H2SO4)=3︰1。若以石墨电极电解该溶液,下列推断中不正确的是 ( )
| A.阴极产物为H2 | B.阳极先析出Cl2,后析出O2 |
| C.电解液的pH不断增大,最终大于7 | D.整个电解的过程实质是电解水 |