如将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2即构成甲烷燃料电池。已知通入甲烷的一极,其电极反应为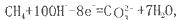 ,下列叙述正确的是
,下列叙述正确的是
| A.通入甲烷的一极为正极 |
| B.通入氧气的一极发生氧化反应 |
C.该电池总反应为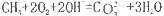 |
| D.该电池在工作时,溶液中的阴离子向正极移动 |
将纯锌片和纯铜片按下图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是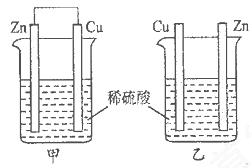
| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的酸性均减弱 | D.产生气泡的速率甲比乙慢 |
储氢合金表面镀铜过程发生反应Cu2++2HCHO+4OH-=Cu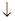 +H2
+H2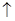 +2H2O+2HCOO-,下列说法错误的是
+2H2O+2HCOO-,下列说法错误的是
| A.电镀过程中氢气在镀件表面析出 |
| B.电镀时溶液中Cu2+移向阴极,并在阴极上发生还原反应 |
| C.阳极反应式为HCHO+3OH--2e-=2H2O+HCOO- |
| D.电镀时每生成6.4g铜镀层放出2.24L H2 |
如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是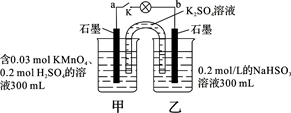
| A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1 |
| B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a |
| C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小 |
| D.乙池中的氧化产物为SO42- |
电化学降解法治理水中硝酸盐的污染原理如图所示。
下列说法正确的是
| A.B为电源正极 |
| B.电解过程中H+ 向阳极移动 |
C.阴极反应式为2NO +6H2O+10e-=N2↑+12OH- +6H2O+10e-=N2↑+12OH- |
| D.理论上电解过程中阴、阳两极产生的气体在同温同压下体积比为2︰5 |
浙江大学的科研小组成功研制出能在“数分钟之内”将电量充满的锂电池,其成本只有传统锂电池的一半。他们把锂锰氧化物(LMO)浸泡在石墨里面,使其变成一个可以导电的密集网络的负极材料(如图),与电解质和正极材料(石墨)构成可充电电池。若电解液为LiAlCl4-SOCl2,电池的总反应为:4LiCl+S+SO2  4Li+2SOCl2。下列说法正确的是
4Li+2SOCl2。下列说法正确的是
| A.电池的电解液可为LiCl水溶液 |
| B.该电池放电时,负极发生还原反应 |
| C.充电时阳极反应式为:4Cl-+S+SO2-4e-=2SOCl2 |
| D.放电时电子从负极经外电路流向正极,再从正极经 |
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
| A.4Fe(OH)2+2H2O+O2═4Fe(OH)3 |
| B.2Fe+2H2O+O2═2Fe(OH)2 |
| C.2H2O+O2+4e-═4OH- |
| D.Fe-3e-═Fe3+ |

 导线
导线