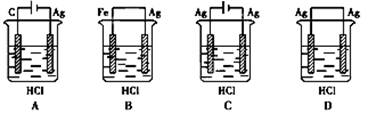
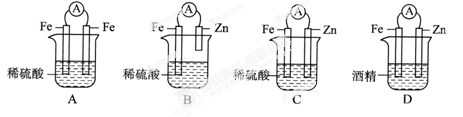
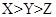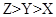一个原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是
| | 正极 | 负极 | 电解质溶液 |
| A | Zn | Cu | CuCl2 |
| B | Zn | Cu | ZnCl2 |
| C | Cu | Zn | CuSO4 |
| D | Cu | Zn | ZnSO4 |
氢氧燃料电池是一种新能源。下图为氢氧燃料电池示意图。下列说法不正确的是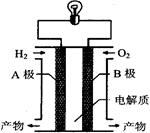
| A.电子由B极通过导线流向A极 |
| B.A极是负极,B极是正极 |
| C.该装置能将化学能转化为电能 |
| D.产物为无污染的水,属于环境友好电池 |
关于如图所示的原电池,下列说法正确的是 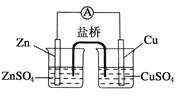
| A.锌电极发生还原反应,铜电极发生氧化反应 |
| B.盐桥中的阴离子向硫酸铜溶液中迁移 |
| C.电子从锌电极通过电流计流向铜电极 |
| D.铜电极上发生的电极反应为2H++2e-===H2↑ |
对铜—锌—稀硫酸组成的原电池装置中,当导线中有1mol电子通过时,理论上的两极变化是①锌片溶解了32.5克 ②锌片增重了32.5克 ③铜片上析出1克氢气④铜片上析出1mol氢气
| A.①③ | B.①④ | C.②③ | D.②④ |
下图所示的装置中,M为活动性顺序位于氢之前的金属,N为石墨棒。下列关于此装置的叙述中,不正确的是( )
| A.N上有气体放出 |
| B.M为负极,N为正极 |
| C.化学能转变为电能的装置 |
| D.导线中有电流通过,电流方向由M到N |
美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200oC左右供电。电池总反应为:C2H5OH+3O2→2CO2+3H2O,下图是该电池的示意图,下列说法正确的是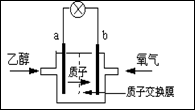
| A.a极为电池的正极 |
| B.电池工作时电流由a极沿导线经灯泡再到b极 |
| C.电池正极的电极反应为:4H+ + O2 + 4e-=2H2O |
| D.电池工作时,1mol乙醇被氧化时就有6mol电子转移 |
用石墨电极电解CuCl2溶液(见下图)。下列分析正确的是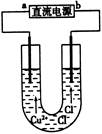
| A.a端是直流电源的负极 |
| B.通电使CuCl2发生电离 |
| C.阳极上发生的反应:Cu2++2e-=Cu |
| D.通电一段时间后,在阴极附近观察到黄绿色气体 |