题目内容
用石墨电极电解CuCl2溶液(见下图)。下列分析正确的是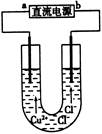
| A.a端是直流电源的负极 |
| B.通电使CuCl2发生电离 |
| C.阳极上发生的反应:Cu2++2e-=Cu |
| D.通电一段时间后,在阴极附近观察到黄绿色气体 |
A
解析试题分析:A、依据装置图可知,铜离子移向的电极为阴极,阴极和电源负极相连,a为负极,正确;B、通电氯化铜发生电解生成氯气和铜,电离是氯化铜离解为阴阳离子,错误;C、与b连接的电极是阳极,氯离子失电子发生氧化反应,电极反应式为:2Cl--2e-=Cl2↑,错误;D、通电一段时间后,氯离子在阳极失电子发生氧化反应,在阳极附近观察到黄绿色气体,错误。
考点:本题考查电解原理。

练习册系列答案
相关题目
高铁电池是电动汽车首选的电池之一,该电池的工作原理为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列关于该电池放电时的说法中正确的是 ( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列关于该电池放电时的说法中正确的是 ( )
| A.高铁电池产生的电流从负极经外电路到达正极 |
| B.正极反应式为Zn+2OH-—2e - =Zn(OH)2 |
| C.负极pH减小,正极pH增大,电解液pH增大 |
| D.每氧化1mol高铁酸钾转移3mol电子 |
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是
| A.未通电前上述镀锌装置可构成原电池,锌为负极,电镀时锌与电源负极相连为阴极 |
| B.电镀时通过1mol电子,阴极上有0.5mol锌的析出 |
| C.未通电前K+向铁极移动,通电后K+还向铁极移动 |
| D.镀锌层破损后对铁制品失去保护作用 |
对铜—锌—稀硫酸组成的原电池装置中,当导线中有1mol电子通过时,理论上的两极变化是①锌片溶解了32.5克 ②锌片增重了32.5克 ③铜片上析出1克氢气④铜片上析出1mol氢气
| A.①③ | B.①④ | C.②③ | D.②④ |
下列叙述正确的是
| A.在原电池的正极和电解池的阳极上发生的都是氧化反应 |
| B.实验室用惰性电极电解NaCl溶液,阴、阳两极收集到的气体体积之比为2∶1 |
C.用铜作电极电解稀硫酸,可能发生反应:Cu+H2SO4 CuSO4+H2↑ CuSO4+H2↑ |
| D.在用惰性电极电解稀硫酸的过程中,溶液pH保持不变 |
