常温时,下列叙述正确的是
| A.稀释pH=10的氨水,溶液中所有离子的浓度均降低 |
| B.pH均为5的HCl和NH4Cl溶液中,水的电离程度相同 |
| C.NaOH和CH3COONa的混合溶液中,c(Na+)+c(H+)═c(OH-)+c(CH3COO-) |
| D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
室温下,向20.00mL 1.000mol·L-1氨水中滴入1.000mol·L-1盐酸,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法错误的是

| A.室温下,a点的氨水电离常数为 |
| B.将此氨水稀释,溶液的导电能力减弱 |
| C.c点时消耗盐酸体积V(HCl)<20mL |
| D.a、d两点的溶液,水的离子积Kw(a)>Kw(d) |
25℃时,在20 mL 0.1 mol·L-1盐酸中逐滴加入0.2 mol·L-1的氨水,溶液的pH与所加氨水的体积关系如图所示,下列有关粒子浓度的关系不正确的是
| A.在b点,盐酸与氨水恰好完全中和 |
| B.在b点:c(H+)=c(OH-),c(NH4+)=c(Cl-) |
| C.在a点:c(Cl-)> c(NH4+)> c(H+)> c(OH-) |
| D.在c点:c(NH4+)+ c(NH3·H2O)="2" c(Cl-) |
下列说法正确的是
| A.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
| B.浓度均为0.1mol·L-1的下列溶液,pH由大到小排列顺序为NaOH>Na2CO3>NaHSO4>(NH4)2SO4 |
| C.pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比为1:2 |
| D.向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
常温下,向10 mL 0.1 mol·L-1的H2C2O4溶液中逐滴加入0.1 mol·L-1 KOH溶液,所得滴定曲线如图所示。下列说法正确的是
| A.KHC2O4溶液呈弱碱性 |
| B.B点时:c(K+)>c(HC2O4-)>c(H+)>c(OH-) |
| C.C点时:c(HC2O4-)+c(C2O42-)+c(H2C2O4)<c(K+)< c(HC2O4-)+2c(C2O42-)+c(H2C2O4) |
| D.D点时:c(H+)+ c(HC2O4-)+ c(H2C2O4)= c(OH-) |
常温下,浓度均为0.1000 mol ? L -1的三种一元酸HX、HY、HZ,分别用0. 1000 mol ? L-1的NaOH溶液进行滴定,滴定曲线如图所示。下列有关叙述正确的是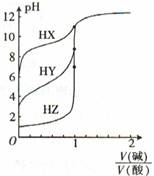
| A.NaOH溶液与三种酸的反应均是吸热反应 |
| B.酸性强弱:HX>HY>HZ |
| C.滴定酸HY可用酚酞作指示剂 |
| D.滴定三种酸都可用甲基橙作指示剂 |
常温时,用0.1000 mol/L NaOH 滴定 25.00 mL 0.1000 mol/L某一元酸HX ,滴定过程中pH 变化曲线如图所示。下列说法正确的是
| A.滴定前,酸中c(H+) 等于碱中c(OH-) |
| B.在A点,c(Na+) > c(X-)> c(HX)> c(H+)> c(OH-) |
| C.在B点,两者恰好完全反应 |
| D.在C点,c(X-) + c(HX) ="0.05" mol/L |
已知:氢氧化镁能溶于浓度均为3mol/L的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是
| A.c(NH4+):③ > ② |
| B.pH:① > ② > ③ |
C.Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s) Mg2+ (aq) + 2OH- (aq)向溶解方向移动 Mg2+ (aq) + 2OH- (aq)向溶解方向移动 |
| D.将等体积的①和③混合,所得溶液中c(Cl-) >c(NH4+) > c(H+) > c(CH3COO-) > c(OH-) |

