碳酸有两个电离常数Ki1、Ki2,分别对应碳酸的两步电离。关于Ki1和Ki2说法正确的是
A.Ki1的表达式为 |
B.Ki2对应的电离过程是HCO3— + H2O 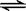 H3O+ + CO32— H3O+ + CO32— |
| C.当碳酸的电离平衡正向移动时,Ki1与Ki2均相应增大 |
| D.改变条件使Ki1减小,则Ki2一定也减小 |
有①②③三瓶体积相等、浓度均为1 mol/L的HCl溶液。将①加热蒸发至体积减少一半,在②中加入少量CH3COONa固体(溶液仍为酸性),③不作改变,然后以酚酞为指示剂,用标准NaOH溶液滴定上述三种溶液,终点时消耗的NaOH溶液的体积大小关系为
| A.①=③>② | B.③>②>① | C.③=②>① | D.①=②=③ |
为比较盐酸与醋酸的酸性强弱,下列方案不可行的是(均在常温下测定)
| A.比较等体积、等pH值的两种溶液的导电性 |
| B.比较等物质的量浓度的氯化钠与醋酸钠溶液的pH值 |
| C.比较等体积、等pH值的两种溶液与过量锌粉反应产生氢气的量 |
| D.比较等体积、等物质的量浓度的两种溶液稀释相同倍数后的pH变化 |
常温下,在l00mL 1mol/L 的NaHCO3溶液中,加入Xmol的Ba(OH)2固体(假设溶液体积和温度保持不变)。以下关于溶液中c(CO32-)及c(HCO3-)的变化判断正确的是
| A.当X=0.025时,溶液中有HCO3-和CO32-,且2C (CO32-) =" C(" HCO3-) |
| B.当X=0.05时,溶液中有HCO3-和CO32-,且C (CO32-)> C( HCO3-) |
| C.当X=0.06时,溶液中HCO3-、CO32-浓度都减小了 |
| D.当X=0.1时,溶液pH增大,沉淀达到最大值 |
常温下pH 的CH3COOH稀溶液与pH
的CH3COOH稀溶液与pH 的NaOH稀溶液等体积混合,下列判断错误
的NaOH稀溶液等体积混合,下列判断错误
的是( )
A.若混合后pH ,则 ,则 |
| B.反应过程中,CH3COOH的电离度增大 |
C.若混合后pH ,则c ,则c <c <c |
D.若混合后CH3COOH与NaOH恰好完全反应,则 |
常温下,对下列四种溶液的叙述正确的是
| | ① | ② | ③ | ④ |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
A.③、④两溶液相比,两者的KW相同
B.①、②两种溶液分别加水稀释100倍,pH变化较大的是①
C.等体积的③、④溶液中分别加入过量锌粒,产生的氢气前者大于后者
D.①、④ 两溶液按2: 1体积比混合后溶液中微粒浓度满足c(NH4+)+c(NH3·H2O)=c(Cl-)
水、双氧水都是由氢、氧元素组成的重要化合物。下列表述正确的是
A.H2O2的电子式为 |
| B.4℃时,纯水的pH<7,溶液呈中性 |
| C.0℃、101kPa,水分子间距:固态>液态 |
| D.101kPa,不同状态水的能量:固态>液态>气态 |
水是最宝贵的资源之一。 下列表述正确的是
A.H2O的电子式为 |
| B.273K、101kPa,水的分子间距离:d(气态)>d(液态)>d(固态) |
| C.4℃时,纯水的pH=7 |
| D.D216O中,质量数之和是质子数之和的两倍 |
在V mL 0.1 mol/L Na2S溶液中逐滴加入V mL 0. 1 mol/L KHSO4溶液,所得溶液中粒子浓度关系正确的是
| A.c(SO42-)= c(HS-) =c(K+) >c(OH-)=c(H+) |
| B.c(Na+)> c(K+)> c(S2-)> c(H+)>c(OH-) |
| C.c(Na+)= c(S2-)+ c(H2S)+c(HS-)+ c(SO42-) |
| D.c(K+)+ c(Na+)+ c(H+)= c(SO42-)+ c(S2-)+ c(HS-)+ c(OH-) |
下列各溶液中,微粒的物质的量浓度关系表述正确的是
| A.0.1 mol/LNa2CO3溶液中:c(Na+)=(HCO3-)+c(H2CO3)+2c(CO32-) |
| B.常温下pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 |
| C.将0.2mol/LNaA溶液和0.1 mol·L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) |
| D.pH=l2的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等 |