已知25℃时,Mg(OH)2的溶度积常数Ksp = 5.6×10-12,MgF2的溶度积常数Ksp =7.4×10-11.下列说法正确的是( )
| A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者c(Mg2+)大 |
| B.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 |
| C.25℃时,Mg(OH)2固体在同体积同浓度的氨水和NH4Cl溶液中的Ksp相比较,前者小 |
| D.25℃时,在Mg(OH)2的悬浊液中加入饱和NaF溶液后,Mg(OH)2不可能转化成MgF2 |
氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是
| A.1mol/L氢氰酸溶液的pH约为3 |
| B.HCN易溶于水 |
| C.10 mL1mol/LHCN恰好与10 mL 1mol/L NaOH溶液完全反应 |
| D.HCN溶液的导电性一定比强酸溶液的导电性弱 |
在相同温度下,100mL 0.1mol·L-1的醋酸与10mL 1mol·L-1的醋酸相比较,下列说法正确的是
| A.溶液中H+的物质的量前者大于后者 |
| B.前者的电离程度小于后者 |
| C.发生中和反应时所需NaOH的量前者大于后者 |
| D.溶液中CH3COOH的物质的量前者大于后者 |
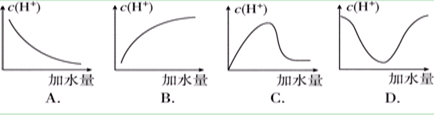
室温下向10 mL c(H+)=10-3 mol·L-1的醋酸溶液中加水稀释后,下列说法正确的是
| A.溶液中导电粒子的数目减少 |
B.溶液中 变大 变大 |
| C.醋酸的电离程度增大,c(OH-)亦增大 |
| D.再加入10 mL c(OH-)=10-3 mol·L-1的NaOH溶液,醋酸与NaOH恰好完全反应 |
水的电离过程为H2O H++OH-,在25℃、35℃时其离子积分别为
H++OH-,在25℃、35℃时其离子积分别为
K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是
| A.水的电离过程是吸热过程 |
| B.c(H+)随着温度的降低而升高 |
| C.在35℃时,纯水中c(H+)>c(OH-) |
| D.水的电离度α(25℃)>α(35℃) |
下列事实可以证明一水合氨是弱电解质的是( )
①0.1 mol/L的氨水可使酚酞溶液变红 ②0.1 mol/L的氯化铵溶液的pH约为5 ③在相同条件下,氨水的导电性比强碱溶液弱 ④氨水受热分解挥发出氨气 ⑤在氨水中存在NH3·H2O分子
| A.①② | B.②③⑤ | C.③④ | D.②④ |
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH ( pOH = —lg c(OH- ) )与pH的变化关系如图所示,则( )
| A.M点所示溶液导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO-)﹥c(Na+) |
| C.M点和N点所示溶液中水的电离程度相同 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是
| A.1mol/L氢氰酸溶液的pH约为3 |
| B.HCN易溶于水 |
| C.10mL 1mol/L HCN恰好与10mL 1mol/L NaOH溶液完全反应 |
| D.HCN溶液的导电性比HCl溶液的弱 |