题目内容
在相同温度下,100mL 0.1mol·L-1的醋酸与10mL 1mol·L-1的醋酸相比较,下列说法正确的是
| A.溶液中H+的物质的量前者大于后者 |
| B.前者的电离程度小于后者 |
| C.发生中和反应时所需NaOH的量前者大于后者 |
| D.溶液中CH3COOH的物质的量前者大于后者 |
A
解析试题分析:由数据可计算前后溶液所含溶质的物质的量均为0.01mol,所以中和所需NaOH的物质的量相等,同时根据平衡理论,浓度越稀电离程度越大,即发生电离的溶质醋酸物质的量越大,电离出的醋酸根离子的物质的量越大,故选A。
考点:本题考查的是电离程度的影响因素。

练习册系列答案
相关题目
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )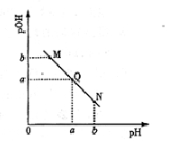
| A.M点所示溶液导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO-)>c(Na+) |
| C.M点和N点所示溶液中水的电离程度相同 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
在0.1mol/L Na2S溶液中,下列关系式正确的是( )
| A.c(Na+)>c(OH-)>c(HS-)>c(S2-) |
| B.c(Na+)+c(H+)=c(HS-)+c(S2-)+c(OH-) |
| C.2c(Na+)=c(H2S)+c(HS-)+c(S2-) |
| D.c(OH-)=c(H+)+2c(H2S)+ c(HS-) |
在1 L 1 mol·L-1的氨水中,下列说法正确的是 ( )
| A.含有1 mol NH3分子? | B.含NH3和NH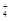 之和为1 mol? 之和为1 mol? |
| C.含NH3·H2O 1 mol? | D.含NH3、NH3·H2O、NH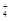 之和为1 mol 之和为1 mol |
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH ( pOH = —lg c(OH- ) )与pH的变化关系如图所示,则( )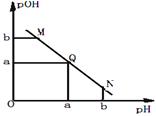
| A.M点所示溶液导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO-)﹥c(Na+) |
| C.M点和N点所示溶液中水的电离程度相同 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
已知一定温度下,有下列难溶电解质的相关数据:
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| KSP/250C | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不正确的是( )
A.向该混合溶液中加过量铁粉,能观察到红色固体析出
B.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
C.该混合溶液中c(SO42-):[c(Cu2+)+ c(Fe2+)+ c(Fe3+)]>5∶4
D.向该混合溶液中加入适量氯水,并调pH至3~4后过滤,能得到纯净的CuSO4溶液
在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是( )
| A.图中五点Kw间的关系:B>C>A=D=E |
| B.C点一定是纯水 |
| C.D点可能是醋酸溶液,E点可能是醋酸钠溶液 |
| D.100℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性 |
0.1mol/L K2CO3溶液中,若使c (CO32—)更接近0.1 mol/L,可采取的措施是
| A.加入少量盐酸 | B.加水 | C.加KOH固体 | D.加热 |
下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
| A.相同浓度的两溶液中c(H+)相同 |
| B.100mL0.1mol/L的两溶液能中和等物质的量的氢氧化钠 |
| C.pH=3的两溶液都稀释10倍,盐酸的pH大于醋酸的PH |
| D.两溶液中分别加人少量对应的钠盐,c(H+)均明显减小 |