将 a g 含NaOH样品溶解在 b mL 0.l mol·L-1的硫酸中,再加入 c mL 0.1 mol·L-1 的氢氧化钡溶液,反应后所得溶液恰好呈中性,则样品中NaOH的纯度是( )
| A.[(b-c)/125a]×100% | B.[(b-2c)/125a]×100% |
| C.[(b-c)/250a]×100% | D.[(8b-8c)/a]×100% |
室温下,下列溶液等体积混和,所得溶液pH的一定大于7的是( )
| A.0.1mol.l-1盐酸溶液和0.1mol.l-1氢氧化钠溶液 |
| B.0.1mol.l-1盐酸溶液和0.1mol.l-1氢氧化钡溶液 |
| C.pH =4醋酸溶液和pH =10氢氧化钠溶液 |
| D.pH =4盐酸溶液和pH =10氢氧化钡溶液 |
在0.1mol/L Na2S溶液中,下列关系式正确的是( )
| A.c(Na+)>c(OH-)>c(HS-)>c(S2-) |
| B.c(Na+)+c(H+)=c(HS-)+c(S2-)+c(OH-) |
| C.2c(Na+)=c(H2S)+c(HS-)+c(S2-) |
| D.c(OH-)=c(H+)+2c(H2S)+ c(HS-) |
向三份0.1 mol·L-1CH3COONa溶液中分别加入少量NH4NO3固体、Na3PO4固体、HCl气体(忽略溶液体积变化),则CH3COO-浓度的变化依次为( )
| A.减小、增大、减小 | B.增大、减小、减小 |
| C.减小、增大、增大 | D.增大、减小、增大 |
下列水解的离子方程式正确的是
A.S2-+2H2O H2S+2OH- H2S+2OH- | B.Fe3++3H2O Fe(OH)3+3H+ Fe(OH)3+3H+ |
| C.CO32-+H2OHCO3-+OH- | D.HS-+H2O H2S↑+OH- H2S↑+OH- |
0.1 mol / L Na2CO3和0.1 mol / L NaHCO3溶液的pH值比较( )
| A.大于 | B.等于 | C.小于 | D.不能肯定 |
等物质的量浓度的下列溶液中,NH4+离子的浓度最大的是( )
| A.NH4Cl | B.NH4HCO3 | C.NH4HSO4 | D.NH4NO3 |
下列物质的水溶液,其中PH值小于7的是( )
| A.Na2CO3 | B.NH4NO3 | C.Na2SO4 | D.KNO3 |
H2S水溶液中存在电离平衡H2S H++HS– 和HS–
H++HS– 和HS– H++S2–。下列说法正确的是
H++S2–。下列说法正确的是
| A.加水,平衡向右移动,溶液中氢离子浓度增大 |
| B.通入过量SO2气体,平衡向左移动,溶液pH值增大 |
| C.滴加新制氯水,平衡向左移动,溶液pH值减小 |
| D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小 |
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成: ①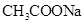 与
与 ②
② 与NaOH ③
与NaOH ③ 与
与 ④
④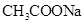 与
与 ,下列各项排序正确的是
,下列各项排序正确的是
| A.pH:②>③>④>① | B. :②>④>③>① :②>④>③>① |
| C.溶液中c(H+): ①>③>②>④ | D. : ①>④>③>② : ①>④>③>② |