题目内容
下列水解的离子方程式正确的是
A.S2-+2H2O H2S+2OH- H2S+2OH- | B.Fe3++3H2O Fe(OH)3+3H+ Fe(OH)3+3H+ |
| C.CO32-+H2OHCO3-+OH- | D.HS-+H2O H2S↑+OH- H2S↑+OH- |
B
解析试题分析:A、S2?分步水解,错误;B、Fe3+水解生成Fe(OH)3和H+,正确;C、CO32?部分水解,应该用 ,错误;D、HS?微弱水解,生成少量H2S,不能用↑符号,错误。
,错误;D、HS?微弱水解,生成少量H2S,不能用↑符号,错误。
考点:本题考查水解离子方程式的书写。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
室温下将等物质的量的NaCN和HCN溶于一定量水中,再加入适量稀盐酸,调整溶液pH=7。下列说法正确的是( )
| A.未加入稀盐酸之前:c(HCN)>c(Na+)>c( CN-) >c(OH-)>c(H+) |
| B.加稀盐酸后溶液中c(CN-)+c(HCN)= c(Na+) |
| C.pH=7时,溶液中:c( Na+)=" c(" CN-) |
| D.加稀盐酸后H2O的电离程度减小 |
下列对于溶液中的问题叙述正确的是( )
| A.向冰醋酸中加水至配成醋酸稀溶液的过程H+的浓度逐渐减小 |
| B.在稀溶液中:H+(aq) + OH-(aq) = H2O(l); △H=-57.3kJ/mol,则含1 mol HClO的稀溶液和含1 mol KOH的稀溶液完全反应放出的热量等于57.3 kJ |
| C.常温时,pH=2的CH3COOH溶液和HCl溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离的c(H+)相等 |
| D.常温下,将稀NaOH溶液与CH3COOH溶液混合,可能出现pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)的情况 |
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中
c(H+)/c(CH3COOH)值增大,可以采取的措施是 ( )
| A.加少量烧碱溶液 | B.降低温度 | C.加少量冰醋酸 | D.加水 |
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成: ①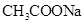 与
与 ②
② 与NaOH ③
与NaOH ③ 与
与 ④
④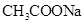 与
与 ,下列各项排序正确的是
,下列各项排序正确的是
| A.pH:②>③>④>① | B. :②>④>③>① :②>④>③>① |
| C.溶液中c(H+): ①>③>②>④ | D. : ①>④>③>② : ①>④>③>② |
室温时,将x mL pH="a" 的稀NaOH溶液与ymL pH=b的稀盐酸充分反应。下列关于反应后溶液pH的判断,正确的是( )
| A.若x=y,且a+b=14,则pH>7 | B.若10x=y,且a+b=13,则pH=7 |
| C.若ax=by,且a+b=13,则pH=7 | D.若x=10y,且a+b=14,则pH>7 |
对于0.1mol·L-1 Na2SO3溶液,正确的是( )
| A.升高温度,溶液的pH降低 |
| B.c(Na+)=2c(SO32—)+ c(HSO3—)+ c(H2SO3) |
| C.c(Na+) + c(H+) = 2c(SO32—)+ 2c(HSO3—) + c(OH—) |
| D.加入少量NaOH固体,c(SO32—)与c(Na+)均增大 |
水的电离过程为H2O H++OH-,在25℃、35℃时其离子积分别为
H++OH-,在25℃、35℃时其离子积分别为
K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是
| A.水的电离过程是吸热过程 |
| B.c(H+)随着温度的降低而升高 |
| C.在35℃时,纯水中c(H+)>c(OH-) |
| D.水的电离度α(25℃)>α(35℃) |
下列关于盐酸与醋酸两种稀溶液的说法正确的是 ( )
| A.相同浓度的两溶液中c(H+)相同 |
| B.100mL0.1mol/L的两溶液能中和等物质的量的氢氧化钠 |
| C.pH=3的两溶液都稀释10倍,盐酸的pH大于醋酸的PH |
| D.两溶液中分别加人少量对应的钠盐,c(H+)均明显减小 |