题目内容
在0.1mol/L Na2S溶液中,下列关系式正确的是( )
| A.c(Na+)>c(OH-)>c(HS-)>c(S2-) |
| B.c(Na+)+c(H+)=c(HS-)+c(S2-)+c(OH-) |
| C.2c(Na+)=c(H2S)+c(HS-)+c(S2-) |
| D.c(OH-)=c(H+)+2c(H2S)+ c(HS-) |
D
解析试题分析:A、S2?少量分步水解,所以离子浓度大小顺序为:c(Na+)>c(S2?)>c(OH?)>c(HS?),错误;B、根据电荷守恒可得:c(Na+)+c(H+)=c(HS?)+2c(S2?)+c(OH?),错误;C、根据物料守恒可得:c(Na+)=2c(H2S)+2c(HS?)+2c(S2?),错误;D、根据质子守恒可得c(OH-)=c(H+)+2c(H2S)+ c(HS-),正确。
考点:本题考查离子浓度比较。

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
常温下,用 0.10 mol·L-1 NaOH溶液分别滴定20.00 mL 0.10 mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如下图所示,则下列说法正确的是( )

图1 图2
| A.图2是滴定盐酸的曲线 |
| B.a与b的关系是:a<b |
| C.E点对应离子浓度由大到小的顺序为: c(CH3COO-)> c(Na+)> c(H+)> c(OH-) |
| D.这两次滴定都可以用甲基橙作为指示剂 |
已知:在100℃时,水的离子积为1×10-12,此时将pH=12的NaOH溶液V1 L与pH=l的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1∶V2为( )
| A.1 : 9 | B.10: 1 | C.9 : 1 | D.1: 10 |
下列物质的水溶液,其中PH值小于7的是( )
| A.Na2CO3 | B.NH4NO3 | C.Na2SO4 | D.KNO3 |
关于溶液的酸碱性说法正确的是( )
| A.c(H+)很小的溶液一定呈碱性 |
| B.PH=7的溶液一定呈中性 |
| C.c(OH-)= c(H+)的溶液一定呈中性 |
| D.不能使酚酞试液变红的溶液一定呈酸性 |
水的电离平衡曲线如图所示,下列说法不正确的是( )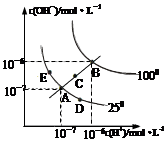
| A.图中五点KW间的关系:B>C>A=D=E |
| B.若从A点到D点,可采用:温度不变在水中加入少量的酸 |
| C.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性 |
| D.若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体 |
在相同温度下,100mL 0.1mol·L-1的醋酸与10mL 1mol·L-1的醋酸相比较,下列说法正确的是
| A.溶液中H+的物质的量前者大于后者 |
| B.前者的电离程度小于后者 |
| C.发生中和反应时所需NaOH的量前者大于后者 |
| D.溶液中CH3COOH的物质的量前者大于后者 |
下列叙述中正确的是
| A.加热蒸干灼烧FeCl3溶液,最后所得固体为Fe(OH)3 |
| B.将pH=4的醋酸溶液稀释后,溶液中所有离子浓度都降低 |
| C.pH相同,体积相同的醋酸溶液和稀硫酸分别与足量锌充分反应,产生氢气的量相同 |
| D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB |