常温下,下列离子能使纯水中的H+离子数目增加的是
| A.NH4+ | B.CO32- | C.S2- | D.Na+ |
相同温度下等物质的量浓度的下列溶液中,pH值最小的是
A. | B. | C.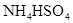 | D. |
下列叙述正确的是
| A.NaHCO3溶液中:c(H+) + c(Na+)=c(HCO3-)+2c(CO32-) + c(OH-) |
| B.pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)一样多 |
| C.0.2mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH=1 |
| D.向10 mL 0.10mol?L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
下列叙述正确的是
| A.将纯水加热,水的离子积变大、pH变小、溶液呈酸性 |
| B.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| C.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)相等 |
| D.中和体积和pH都相等的HCl溶液和CH3COOH溶液,所消耗的NaOH物质的量相同 |
已知醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则下列说法正确的是
| A.实现该变化的只能是升高温度 | B.溶液的导电能力一定变强 |
| C.溶液的pH一定减小 | D.发生电离的分子总数增多 |
已知某温度下,几种酸的电离常数如下:Ka(HCN)= 6.2×10-10 mol/L、Ka(HF)= 6.8×10-4 mol/L、Ka(CH3COOH)= 1.8×10-5 mol/L、Ka(HNO2)= 6.4×10-6mol/L。则物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是
| A.NaCN | B.NaF | C.CH3COONa | D.NaNO2 |
为证明某可溶性一元酸(HX)是弱酸,有如下实验方案,其中不合理的是
| A.室温下,测0.1 mol/L HX溶液的pH,若pH>1,证明HX是弱酸 |
| B.室温下,测1 mol/L NaX溶液的pH,若pH>7,证明HX是弱酸 |
| C.相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相串联的灯泡较暗,证明HX为弱酸 |
| D.将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 |
下列操作中,能使电离平衡H2O H++OH-向右移动且溶液呈酸性的是
H++OH-向右移动且溶液呈酸性的是
| A.向水中加入NaHSO4溶液 | B.向水中加入Al2(SO4)3固体 |
| C.向水中加入Na2CO3溶液 | D.将水加热到100℃,使pH=6 |
已知:pAg=-lg{c(Ag+)},KspAgCl=1×10-12如图是向10mLAgNO3溶液中逐渐加入0.1 mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线)。根据图象所得下列结论正确的是( )
(提示:KspAgCl>KspAgI)
| A.原AgNO3溶液的物质的量浓度为0.1 mol·L-1 |
| B.图中x点的坐标为(100,6 ) |
| C.图中x点表示溶液中Ag+ 与Cl- 浓度相同 |
| D.把0.1 mol·L-1的NaCl换成0.1 mol·L-1NaI则图象在终点后变为虚线部分 |
下列溶液中有关物质的浓度关系正确的是 ( )
| A.c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4) >c[(NH4)2SO4]>c(NH4Cl) |
| B.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C.1.0 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| D.某二元弱酸酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |