有4种混合溶液,分别由等体积0.1 mol·L﹣1的两种溶液混合而成,①NH4Cl与CH3COONa
②NH4Cl与HCl③NH4Cl与NaCl④NH4Cl与NH3·H2O(混合液呈碱性)。下列各项排序正确的是( )
| A.pH:②<①<③<④ |
| B.c(NH4+):①<③<②<④ |
| C.溶液中c(H+):①<③<②<④ |
| D.c(NH3·H2O):①<③<④<② |
常温下,下列各组比值为1:2的是( )
| A.0.1 mol/L与0.2 mol/L醋酸溶液,c (H+)之比 |
| B.0.1 mol/L NaHCO3溶液,c(HCO3﹣)与c(Na+)之比 |
| C.pH=10的Ba(OH)2溶液与氨水,溶质的物质的量浓度之比 |
| D.pH=3的硫酸与醋酸溶液,c(SO42﹣)与c(CH3COO﹣)之比 |
下列说法不正确的是
| A.将pH=4的某酸稀释10倍,测得其pH<5,则该酸为弱酸 |
B.0.1mol 的NaHCO3溶液中 的NaHCO3溶液中 |
C.0.1mol 的NaHA溶液Ph=5,则溶液: 的NaHA溶液Ph=5,则溶液: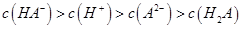 |
D.pH=4的醋酸与pH=10的氢氧化钠溶液等体积混合,所得溶液 |
下列叙述正确的是
| A.0.1mol·L-1CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大 |
| C.pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)不相等 |
D.在NaHCO3溶液中:c(OH-)+c( )=c(H+)+c(H2CO3) )=c(H+)+c(H2CO3) |
在相同温度下,100 mL0.01 mol·L-1的醋酸溶液与10 mL0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是
| A.中和时所需NaOH的量 | B.电离的程度 |
| C.H+的物质的量浓度 | D.CH3COOH的物质的量 |
下列说法正确的是
| A.0.1 mol/L溶液中的(NH4)2SO4,溶液中的c(NH4+)<c(SO42-) |
| B.相同温度下,0.6 mol/L氨水溶液与0.3 mol/l氨水溶液中c(OH-)之比是2:1 |
| C.向0.1 mol/LNaNO3溶液中滴加硝酸使溶液pH=5,此时混合液中的c(Na+)<c(NO3-) |
| D.向醋酸钠溶液中加入适量醋酸,使混合液的pH=7,此时混合液中c(Na+)<c(CH3COO-) |
Na2SO3溶液做为吸收液吸收SO2时,吸收液pH随n( ): n(
): n( )变化的关系如下表:
)变化的关系如下表:
n( ): n( ): n( ) ) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
以下离子浓度关系的判断正确的是
A.NaHSO3溶液中c(H+) < c (OH-)
B.Na2SO3溶液中c(Na+)> c (
 )> c (
)> c ( ) > c (OH-) > c(H+)
) > c (OH-) > c(H+) C.当吸收液呈中性时,c(Na+) >c (
 ) > c (
) > c ( ) > c (OH-) = c(H+)
) > c (OH-) = c(H+) D.当吸收液呈中性时,c(Na+)>c (
 )+c (
)+c ( )
) 在常温下,0.1000mol·L-1Na2CO3溶液25mL 用0.1000mol·L-1盐酸滴定,其滴定曲线如图。对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是
| A.a点:c(CO32-)=c(HCO3-)>c(OH-) |
| B.b点:5c(Cl-)>4c(HCO3-)+4c(CO32-) |
| C.c点:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| D.d点:c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
25℃时,下列溶液中水的电离程度最小的是
| A.0.01 mol/L NaHSO4 | B.0.1 mol/L Na2CO3溶液 |
| C.pH = 4盐酸溶液 | D.pH =11氨水 |