在一固定容积的密闭容器中进行如下反应:2SO (g)+O
(g)+O (g)
(g) 2SO
2SO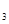 (g),已知反应进行到10秒时,SO
(g),已知反应进行到10秒时,SO 、O
、O 、SO
、SO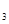 的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是
的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是
A.10秒时,用O 表示该反应的平均反应速率为0.01 mol/(L·s) 表示该反应的平均反应速率为0.01 mol/(L·s) |
B.当反应达平衡时,SO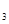 的物质的量可能为0.4 mol 的物质的量可能为0.4 mol |
C.当SO 和O 和O 的生成速率之比为2:1时,达到该反应限度 的生成速率之比为2:1时,达到该反应限度 |
D.向容器内充人SO ,可以提高反应速率 ,可以提高反应速率 |
已知反应A(g)+3B(g)  2C(g)+D(g),在某段时间内,以A的浓度变化表示的反应速率为2 mol/(L·s),则以C的浓度变化表示的反应速率为
2C(g)+D(g),在某段时间内,以A的浓度变化表示的反应速率为2 mol/(L·s),则以C的浓度变化表示的反应速率为
| A.1 mol/(L·s) | B.3 mol/(L·s) |
| C.4 tool/(L·s) | D.2 mol/(L·s) |
在一定条件下,对于密闭容器中进行的可逆反应:
 2SO3(g)。下列说法不正确的是
2SO3(g)。下列说法不正确的是
| A.改变反应条件可以改变该反应的限度 |
| B.达到平衡后,SO3、SO2、O2在密闭容器中共存 |
| C.达到平衡后,反应停止,正、逆反应速率都等于零 |
| D.SO3、SO2、O2的浓度保持不变,说明该可逆反应达到了平衡状态 |
在某化学反应中,生成物B的浓度在10 s内从1.5 mol/L变成2.0 mol/L,则这10 s内B的平均反应速率是
| A.0.05 mol/(L·s) | B.0.05 mol/L |
| C.0.20 mol/(L·s) | D.0.20 mol/L |
某密闭容器中存在2NO+O2 2NO2反应,平衡时NO的转化率与温度变化关系如图所示(曲线上任何一点都表示平衡状态),下列说法中正确的是
2NO2反应,平衡时NO的转化率与温度变化关系如图所示(曲线上任何一点都表示平衡状态),下列说法中正确的是
| A.该反应的正反应是吸热反应 |
| B.若温度为T1、T3时的平衡常数分别为K1、K3,则K1<K3 |
| C.T1时,当反应处于D点,则该反应的逆反应速率大于正反应速率 |
| D.如果缩小容器体积,则平衡时表示NO转化率与温度变化关系的曲线在原曲线上方 |
在容积为2L的密闭容器中进行反应:CO(g)+2H2(g) CH3OH(g) ,其他条件不变,在300℃和500℃时,甲醇物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是( )
CH3OH(g) ,其他条件不变,在300℃和500℃时,甲醇物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是( )
| A.该反应的△H>0 |
| B.其他条件不变,升高温度反应的平衡常数增大 |
C.300℃时,0-t 1min内 CH3OH的平均生成速率为 mol·L-1 min-1 mol·L-1 min-1 |
D.A点的反应体系从300℃升高到500℃,达到平衡时 减小 减小 |
为了探索外界条件对反应:aX(g)+bY(g) cZ(g) 的影响,将X和Y以物质的量之比为a∶b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。 下列判断正确的是( )
cZ(g) 的影响,将X和Y以物质的量之比为a∶b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。 下列判断正确的是( )
| A.△H<0, a+b>c | B.△H>0, a+b<c |
| C.△H>0, a+b>c | D.△H<0, a+b<c |
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
下列说法正确的是( )
| A.上述生成Ni(CO)4(g)的反应为吸热反应 |
B.25℃时反应Ni(CO)4(g)  Ni(s)+4CO(g)的平衡常数为0.5(mol·L-1)3 Ni(s)+4CO(g)的平衡常数为0.5(mol·L-1)3 |
| C.在某条件下达到平衡,测得Ni(CO)4、CO浓度均为0.5mol/L,则此时温度高于80℃ |
| D.80℃达到平衡时,保持体积不变,往体系中充入一定量的CO,再次达到平衡后CO的体积分数减小 |
下列图示与对应的叙述相符的是



甲 乙 丙 丁
A.图甲可以判断出反应A(g) + B(g) 2C(g) 的△H<0,T2>T1 2C(g) 的△H<0,T2>T1 |
B.图乙表示压强对可逆反应2A(g) + 2B(g) 3C(g) + D(s)的影响,乙的压强比甲的压强大 3C(g) + D(s)的影响,乙的压强比甲的压强大 |
| C.据图丙,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH≈4 |
| D.图丁表示25℃时,用0.1 mol·L—1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入盐酸体积的变化 |
 CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动