一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
| | 甲 | 乙 | 丙 | 丁 | |
| 密闭容器体积/L | 2 | 2 | 2 | 1 | |
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2的平衡转化率/% | 80 | α1 | α2 | α3 | |
下列判断中,正确的是
A.甲中反应的平衡常数小于乙
B.该温度下,甲和乙中反应的平衡常数K均为400
C.SO2的平衡转化率:α1>α2=α3
D.容器中SO3的物质的量浓度:丙>甲=丁
下列说法正确的是
| A.除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤 |
| B.某温度时,纯水中c(H+)=2×10-7mol·L-1,则c(OH-)=5×10-8mol·L-1 |
C.N2(g)+3H2(g) 2NH3(g),其他条件不变,增大压强,v(正)增大而v(逆)减小 2NH3(g),其他条件不变,增大压强,v(正)增大而v(逆)减小 |
D.Na2CO3溶液中存在平衡:CO32-+H2O HCO3-+OH一,升高温度溶液碱性增强 HCO3-+OH一,升高温度溶液碱性增强 |
下列有关说法正确的是
| A.锌与稀硫酸反应时加入少量硫酸铜,反应加快的原因是Cu2+水解增大了H+浓度 |
| B.增大醋酸溶液的浓度,溶液中c(OH-)减小的原因是水的离子积Kw减小 |
| C.pH=3的盐酸与pH=11的LiOH溶液等体积混合溶液呈碱性,说明LiOH为强碱 |
| D.TATP(C8H18O6)受撞击分解爆炸,且无明显热效应,说明该分解反应熵显著增加 |
化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是

A.图①表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| B.图②表示向乙酸溶液中通入氨气至过量的过程,溶液导电性的变化 |
| C.图③表示在1 L 1 mol/L FeBr2溶液中通入Cl2时Br-的量的变化 |
| D.图④表示一定浓度Na2CO3溶液中滴加盐酸,生成CO2与滴加盐酸的物质的量的关系 |
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g) + 2B(g) xC(g)ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是 ( )
xC(g)ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是 ( )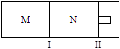
| A.若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N) |
| B.若x>3,达到平衡后B的转化率关系为:α(M)>α(N) |
| C.若x<3,C的平衡浓度关系为:c(M)>c(N) |
| D.x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等 |
物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2 2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是
2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是
| A.反应在前10 min内的平均速率为ν(t-BuNO)=0.0325mol·L-1·min-1 |
| B.保持其他条件不变,若此时再向溶液中加入0.50 mol (t-BuNO)2,重新达平衡时(t-BuNO)2的百分含量减小 |
| C.保持其他条件不变,若该反应在CCl4中进行,其平衡常数为1.9,则(t-BuNO)2的平衡转化率小于65% |
| D.保持其他条件不变,升高温度, (t-BuNO)2的平衡转化率大于65%,则其能量关系可用下图表示 |

向甲、乙、丙三个密闭容器中充人一定量的A和B,发生反应:xA(g)+B(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示 ( )
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1. 0L |
| 温度/ | T1 | T2 | T3 |
| 反应物 起始量 | 0.5molA 1.5 molB | 0.5 molA 1.5 molB | 2.0 molA 6.0 molB |
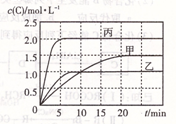
下列说法正确的是
A.由图可知:T1<T2,且该反应为吸热反应
B.T2时该反应的平衡常数K=0.8
C.l0min内甲容器中反应的平均速率v(B)=0.025mol·(L·min)-1
D.T1℃,若起始时甲容器中充入1.5molA、0.5molB,平衡时B的转化率为25%
下列有关说法正确的是 ( )
| A.反应:2CO(g) +2NO(g) |
B.0.1mol·L-1'Na2 CO3溶液加蒸馏水稀释,CO '的水解程度变大,溶液的pH不断增大 '的水解程度变大,溶液的pH不断增大 |
| C.电解精炼铜过程中,阳极质量的减少量与阴极质量的增加量一定相等 |
D.C(s) +CO2(g) 2CO(g)△H>0,其他条件不变时升高温度,反应速率v(CO2)和CO2的平衡转化率均增大 2CO(g)△H>0,其他条件不变时升高温度,反应速率v(CO2)和CO2的平衡转化率均增大 |
900℃时,向2.0L恒容密闭容器中充入0.40mol乙苯,发生反应: ΔH=a kJ·mol—1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
ΔH=a kJ·mol—1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(乙苯)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(苯乙烯)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前20 min的平均速率为v(H2)=0.008mol·L-1·min-1
B.保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08mol·L-1,则a<0
C.保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率为50.0%
D.相同温度下,起始时向容器中充入0.10mol乙苯、0.10mol苯乙烯和0.30molH2,达到平衡前v正>v逆
 zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是