T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的浓度变化如图(Ⅰ)所示。保持其它条件不变,在T1、T2两种温度下,Y的体积分数变化如图(Ⅱ)所示,下列结论正确的是( )
| A.图(Ⅱ)中T1>T2,则正反应是吸热反应 |
| B.t2 min时,保持压强不变,通入稀有气体,平衡向正反应方向移动 |
| C.其它条件不变,升高温度,正、逆反应速率均增大,且X的转化率增大 |
| D.T℃时,若密闭容器中各物质起始浓度为:0.4 mol·L-1X、0.4 mol·L-1 Y、0.2mol/LZ保持其他 |
一定温度下,在一固定体积的容器中,通人一定量的CO和H2O,发生如下反应:CO(g)十H2O(g) CO2(g)十H2 (g) △H<0。在850℃时,CO和H2O浓度变化如下左图;若在t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。下列说法正确的是:
CO2(g)十H2 (g) △H<0。在850℃时,CO和H2O浓度变化如下左图;若在t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。下列说法正确的是:
| A.850℃时,按左图所示0~4min用CO2表示的平均反应速率v(CO2)=0.02mol·L-1·min-1 |
| B.t1℃高于850℃ |
| C.t1℃时,反应在4min~5min间,平衡向逆反应方向移动,若其它条件不变,可能的原因是增大压强 |
| D.若t2℃时,各物质的平衡浓度符合c(CO2)·c(H2)=2 [c(CO)·c(H2O)],则t2℃高于850℃ |
汽车尾气净化中的一个反应如下:2NO(g)+2CO(g) N2(g)+2CO2(g) △H=-373.4kJ/mol
N2(g)+2CO2(g) △H=-373.4kJ/mol
反应达到平衡后,改变某一个条件,下列示意图曲线①?⑧中正确的是
| A.①⑥⑧ | B.①⑤⑦ | C.②③④ | D.③⑥⑦ |
把CoCl2溶解于浓盐酸中,溶液中存在下列平衡:
Co2+ + 4Cl— CoCl4— △H>0
CoCl4— △H>0
粉红色 蓝色
有关上述可逆反应的下列说法不正确的是 ( )
| A.对溶液所在体系加热,溶液蓝色加深 |
| B.对溶液所在体系用冰水降温,上述反应的平衡常数减小 |
| C.室温下,加水稀释,上述反应的平衡常数减小 |
| D.室温下,加水稀释至一定范围,溶液为粉红色 |
铁的氧化物可用于脱除煤气中的H2S,该反应原理为:
①Fe3O4 (s)+3H2S(g)+H2 (g) 3FcS(s)+4H2O(g) △H=a kJ ? mol-1
3FcS(s)+4H2O(g) △H=a kJ ? mol-1
②Fe2O3(s)+2H2S(g) + H2(g) 2FeS(s)+3H2O(g) △H=bkJ ? mol-1
2FeS(s)+3H2O(g) △H=bkJ ? mol-1
③FeO(s)+H2S(g)  FeS(s)+H2O(g) △H=ckJ· mol-1
FeS(s)+H2O(g) △H=ckJ· mol-1
温度与平衡常数的关系如图,下列有关说法正确的是
| A.a、b、c均小于0 |
| B.压强越大,H2S的脱除率越高 |
| C.温度越高,H2S的脱除率越高 |
| D.反应①、②、③的平衡常数表达式相同 |
将CO2转化为甲醇的原理为 CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH <0 。500 ℃时,在体积为1 L的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是
CH3OH(g)+H2O(g) ΔH <0 。500 ℃时,在体积为1 L的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是
| A.曲线X可以表示CH3OH(g) 或H2O(g) 的浓度变化 |
| B.从反应开始到10min时,H2的反应速率v(H2)=0.225mol/(L﹒min) |
| C.平衡时H2的转化率为75% |
| D.500 ℃时该反应的平衡常数K=3 |
工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g) +H2O(g)=CO(g) +3H2(g) △H>0,在一定条件下,向体积为1L的密闭容器中充入1 mol CH4(g)和1mol H2O(g),测得H2O(g)和H2(g)的浓度随时间变化曲线如图所示,下列说法正确的是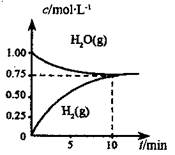
| A.达平衡时,CH4( g)的转化率为75% |
| B.0~10 min 内,v(CO)=0.075 mol?L-1·min-1 |
| C.该反应的化学平衡常数K=0.1875 mol?L-1 |
| D.当CH4(g)的消耗速率与H2O(g)的生成速率相等,反应到达平衡 |
 2SO2(g)+O2(g)
2SO2(g)+O2(g)
