据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实,其反应的化学方程式为:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) 。 下列叙述正确的是
CH3CH2OH(g)+3H2O(g) 。 下列叙述正确的是
| A.当v(CO2)=2v(CH3CH2OH)时,反应一定达到平衡状态 |
| B.当平衡向正方向移动时,平衡常数一定增大 |
| C.增大压强,可提高CO2和H2的转化率 |
| D.相同条件下,2 mol氢原子所具有的能量等于1 mol氢分子所具有的能量 |
在一定温度下,饱和氯水中存在平衡:Cl2+H2O H++Cl-+HClO。下列说法中确的是
H++Cl-+HClO。下列说法中确的是
A.光照一段时间后,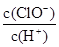 增大 增大 |
| B.加入碳酸钙粉末后,溶液的pH增大 |
| C.加入少量水,由水电离的c(H+)减小 |
| D.加入NaOH固体,一定有c(Na+)>c(Cl-)>c(H+)>c(ClO-)) |
在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1)
2NH3(g) △H=-92.4 kJ·mol-1)
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1 mol N2、3 mol H2 | 4 mol NH3 |
| NH3的浓度(mol·L-1) | c1 | c2 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ |
| 气体密度 | ρ1 | ρ2 |
| 反应物转化率 | α1 | α2 |
下列说法正确的是
A.c1<c2<2 c1 B.a+b>92.4 C.α1 +α2=1 D.ρ2=2ρ1
下列图示与对应的叙述不相符的是
| A.图1表示相同温度下,向pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH的变化曲线,其中a表示氨水稀释时pH的变化曲线 |
| B.图2表示向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸所得沉淀物质的量与盐酸体积的关系 |
C.图3表示压强对可逆反应CO(g)+H2O(g) CO2(g)+H2(g)的影响,乙的压强比甲的压强大 CO2(g)+H2(g)的影响,乙的压强比甲的压强大 |
| D.图4表示10 mL 0.01 mol·L-1 KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4 溶液混合时,n(Mn2+) 随时间的变化(Mn2+对该反应有催化作用) |
下列图示与对应的叙述相符的是
A.图I可表示N2+3H2 2NH3的速率时间图像,t1时刻改变的条件是升高温度 2NH3的速率时间图像,t1时刻改变的条件是升高温度 |
| B.图Ⅱ可表示用0.1 000 mol/L醋酸滴定40.00 mL0.1000 mol/LNaOH溶液得到的滴定曲线 |
| C.图Ⅲ可表示NO2平衡转化率与温度、压强的变化关系,由图可知:△H<0、P1<P2 |
| D.图Ⅳ可表示pH相同的NaOH溶液与氨水稀释过程的pH变化.其中曲线a对应氨水 |
一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应,在t1时达到平衡:
A(g)+ B(g) xC(g)+D(s)。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变
xC(g)+D(s)。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变
化如图所示。有关说法正确的是
| A.反应方程式中x=2 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量D |
| D.t1~t3间该反应的平衡常数相同 |
下列事实不能用勒夏特列原理解释的是
| A.配制氯化铁溶液时,加入少量稀盐酸 |
| B.配制氯化亚铁溶液时,加入少量铁屑 |
| C.在含有酚酞的氨水中加入少量NH4Cl,溶液颜色会变浅 |
| D.在硫酸铜饱和溶液中加入一块胆矾,晶体外形变规则 |
温度为T时,向2.0L恒容密闭容器中充入1.0 molPCl5,反应PCl5(g) PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
以下对反应过程的分析和判断正确的是
A. 反应在前50 s的平均速率为v(PCl3)="0.0032" mol·L-1·s-1
B.保持其他条件不变,若升高温度,平衡时,c(PCl3)="0.11" mol·L-1,则反应为放热反应
C. 相同温度下,若起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,则达平衡前v(正)>v(逆)
D.相同温度下,若起始时向容器中充入2.0molPCl3、2.0molCl2,则达平衡时,PCl3的转化率大于80%
在密闭容器中进行反应:2A(g)+B(g) 3C(g)+Q(Q>0)。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
3C(g)+Q(Q>0)。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是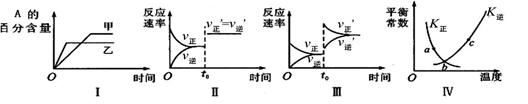
| A.图I表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻缩小容器体积对反应速率的影响 |
| C.图Ⅲ表示t0时刻增大B浓度对反应速率的影响 |
| D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |
已知:(CH3COOH) 2(g) 2CH3COOH(g)经试验测得在不同压强下体系的平均相对分子质量(M)随温度T的变化曲线如图所示,下列说法正确的是
2CH3COOH(g)经试验测得在不同压强下体系的平均相对分子质量(M)随温度T的变化曲线如图所示,下列说法正确的是
| A.该过程的△H<0 |
| B.平衡常数: K(a)=K(b)<K(c) |
| C.气体压强:P(a)<P(b)= P(c) |
| D.当M=80时,(CH3COOH) 2和CH3COOH的物质的量之比为1:1 |