下列图示与对应的叙述相符的是( )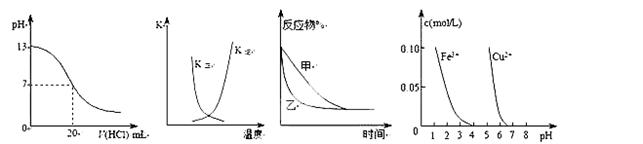
① ② ③ ④
| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化 |
B.图②中曲线表示反应2A(g) + B(g) 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化 |
C.图③表示压强对可逆反应2A(g)+2B(g)  3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| D.据图④若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右。 |
将H2和Br2充入恒容密闭容器中,恒温下发生反应H2(g)+Br2(g) 2HBr(g) △H<0;平衡时Br2的转化率为a,若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b,则a与b的关系是( )。
2HBr(g) △H<0;平衡时Br2的转化率为a,若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b,则a与b的关系是( )。
| A.a>b | B.a=b | C.a < b | D.无法确定 |
下列反应达到平衡后,升高温度可以使混合气体平均相对分子质量增大的是( )
A.H2(g)+I2(g)  2HI(g) ΔH<0 2HI(g) ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
C.N2(g)+3H2(g)  2NH3(g)ΔH<0 2NH3(g)ΔH<0 |
D.2SO3(g) 2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
一定量的锌粉和6mol·L-1的过量盐酸反应,当向其中加入少量的下列物质时,一定能够加快反应速率,又不影响产生H2总量的是( )
①石墨 ②CuO ③铜粉 ④铁粉 ⑤浓盐酸 ⑥无水乙酸
| A.①③④ | B.②④⑥ | C.②⑤⑥ | D.①③⑤ |
在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)
|
B.A、B、C的浓度相等
C.单位时间生成 n mol A,同时生成 3n mol B
D.生成C的速率与C分解的速率相等
决定化学反应速率的主要因素是
| A.反应物的浓度 | B.反应温度 | C.使用催化剂 | D.反应物的性质 |
一定条件下,在固定容积密闭容器中发生可逆反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述中正确的是
4NO(g)+6H2O(g),下列叙述中正确的是
| A.达到化学平衡时,化学反应速率的关系是2v逆(NH3)=3v正 (H2O) |
| B.达到化学平衡时,NH3、O2、NO、H2O物质的量之比为4∶5∶4∶6 |
| C.混合气体的密度一定时,该化学反应达到化学平衡 |
| D.若单位时间内生成x mol NO的同时,生成x mol NH3,则反应达到平衡状态 |