在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g)
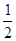 N2(g)+CO2(g);ΔH=-373.2kJ·mol-1
N2(g)+CO2(g);ΔH=-373.2kJ·mol-1
达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时减小压强 |
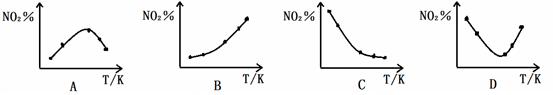
图为某化学反应速率一时间图。在 时刻升高温度或增大压强,都符合下图所示变化的反应是
时刻升高温度或增大压强,都符合下图所示变化的反应是
A.2SO2(g)+O2(g) 2SO3(g);ΔH<0 2SO3(g);ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g);ΔH<0 4NO(g)+6H2O(g);ΔH<0 |
C.H2(g)+I2(g) 2HI(g); ΔH>0 2HI(g); ΔH>0 |
D.C(s)+H2O(g) CO(g)+H2(g) ;ΔH>0 CO(g)+H2(g) ;ΔH>0 |
在一密闭容器中充入一定量的N2和H2,经测定反应开始后的2s内氢气的平均速率:ν(H2)=0.45mol/(L·s),则2s末NH3的浓度为
| A.0.50mol/L | B.0.60mol/L | C.0.45mol/L | D.0.55mol/L |
对于密闭容器中的反应:2SO2(g)+O2(g) 2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是
2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是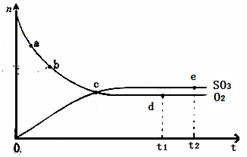
| A.点c处反应达到平衡 |
| B.点a的正反应速率比点b的大 |
| C.点d (t1时刻)和点e (t2时刻)处n(SO2)不一样 |
| D.其他条件不变,600℃时反应至t1时刻,n(SO 3)比上图中的d点值要大 |
COCl2(g)  CO(g) + Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2 分解率的是
CO(g) + Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2 分解率的是
| A.①④⑥ | B.①②④ | C.②③⑥ | D.③⑤⑥ |
已知A(s)+2B(g)  2C(g)+D(g) △H<0 在一密闭容器中反应的υ-t图。t1时,改变了一个条件,下列叙述正确的是
2C(g)+D(g) △H<0 在一密闭容器中反应的υ-t图。t1时,改变了一个条件,下列叙述正确的是
| A.t1时,一定是升高了反应的温度 |
| B.t1时,可能是向容器中通入了一定量的C气体 |
| C.t1时,可能是向容器中加入了催化剂 |
| D.t1时改变外界条件后,该反应的平衡常数可能减小,也可能不变 |
在下列反应中:A2(g)+B2(g) 2AB(g)(正反应放热),当其达到平衡时,在下图的曲线中,符合勒夏特列原理的曲线是
2AB(g)(正反应放热),当其达到平衡时,在下图的曲线中,符合勒夏特列原理的曲线是 
| A.①② | B.③④ | C.① | D.①⑤ |
 2CO; △H1>0,反应速率ν1 N2+3H2
2CO; △H1>0,反应速率ν1 N2+3H2 和
和 的变化是
的变化是