下列事实不能用平衡移动原理解释的是
| A.工业合成氨时使用催化剂 |
| B.配制FeCl3溶液时加入少量的盐酸 |
| C.在Na2CO3溶液中,由水电离出的c(OH-) >1×10-7mol/L |
| D.AgCl在水中的溶解度大于在饱和NaCl溶液中的溶解度 |
工业上利用可逆反应N2(g)+3H2(g)  2NH3(g)合成氨,下列叙述正确的是
2NH3(g)合成氨,下列叙述正确的是
| A.合成氨的适宜条件是高温、高压、催化剂,其中催化剂不改变该反应的逆反应速率 |
| B.恒容通入氩气,使反应体系的压强增大,反应速率一定增大 |
| C.该反应是放热反应,降低温度将缩短反应达到平衡的时间 |
D.在t1、t2时刻,NH3 (g)的浓度分别是c1、c2,则时间间隔t1~t2内,NH3 (g)生成的平均速率为v=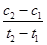 |
在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)  xC(g)+2D(g), 2 min后该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。则下列判断正确的是
xC(g)+2D(g), 2 min后该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。则下列判断正确的是
| A.x=2 |
| B.2 min内A的反应速率为0.6 mol·L-1·min-1 |
| C.B的转化率为40% |
| D.若混合气体的密度不变,则表明该反应达到平衡状态 |
在1 000 K时,已知反应Ni(s)+H2O(g)  NiO(s)+H2(g)的平衡常数K=0.059,当水蒸气和氢气的物质的量浓度相等时,此反应
NiO(s)+H2(g)的平衡常数K=0.059,当水蒸气和氢气的物质的量浓度相等时,此反应
| A.已达平衡状态 | B.未达平衡状态,反应正向进行 |
| C.未达平衡状态,反应逆向进行 | D.无法确定 |
对于反应C(s)+H2O(g)  CO(g)+H2(g) ;ΔH >0,下列有关说法正确的是
CO(g)+H2(g) ;ΔH >0,下列有关说法正确的是
A.平衡常数表达式为K=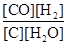 |
| B.增大体系压强,平衡常数K不发生变化 |
| C.升高体系温度,平衡常数K减小 |
| D.增加C(s)的量,平衡正向移动 |
下图表示反应A(g)+B(g) nC(g) △H<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述正确的是
nC(g) △H<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述正确的是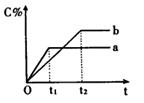
| A.反应由逆反应开始 |
| B.a表示有催化剂,b表示无催化剂 |
| C.若n=2,其它条件相同,a比b的压强大 |
| D.若其它条件相同,a比b的温度高 |
在密闭容器中发生下列反应aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是
| A.A的转化率变大 | B.平衡向正反应方向移动 |
| C.D的质量分数变大 | D.a<c+d |
升高温度,下列数据不一定增大的是
| A.化学反应速率 | B.水的离子积常数Kw |
| C.化学平衡常数 | D.弱酸的电离平衡常数Ka |
可逆反应aA(g)+bB(g) cC(g)+dD(g)符合下图。则下列叙述正确的是
cC(g)+dD(g)符合下图。则下列叙述正确的是

| A.a+b>c+d;正反应放热 |
| B.a+b<c+d;正反应吸热 |
| C.a+b<c+d;正反应放热 |
| D.a+b>c+d;正反应吸热 |
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)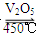 2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是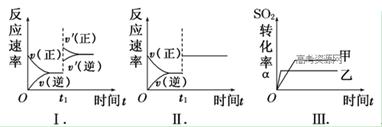
| A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B.图Ⅱ表示的是t1时刻加入催化剂对反应速率的影响 |
| C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化剂效率比乙高 |
| D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |