对于密闭容器中进行的反应:P(g)+ Q(g) R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( )
R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( )
| A.P、Q、R、S的浓度相等 |
| B.P、Q、R、S在密闭容器中共存 |
| C.P、Q、R、S的浓度不再变化 |
| D.用P的浓度表示的化学反应速率与用Q的浓度表示的化学反应速率相等。 |
下列说法正确的是( )
| A.ΔH<0、ΔS>0的反应在温度低时不能自发进行 |
| B.NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57 kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| D.在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向 |
对于某一可逆反应,改变下列条件,一定能使化学平衡发生移动的是( )
| A.增加某反应物的质量 | B.使用催化剂 |
| C.降低反应体系的压强 | D.升高温度 |
在容积为2L的密闭容器中进行反应:CO(g)+2H2(g) CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是
CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是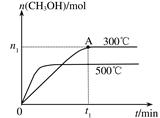
| A.该反应的△H<0 |
| B.其他条件不变,升高温度反应的平衡常数增大 |
C.300℃时,0-t 1min内 CH3OH的平均生成速率为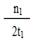 mol·L-1 min-1 mol·L-1 min-1 |
D.A点的反应体系从300℃升高到500℃,达到平衡时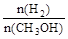 减小 减小 |
从下列事实所得出的解释或结论正确的是
| 选项 | 实验事实 | 解释或结论 |
| A | 2N2O5(g) 4NO2(g)+O2(g) ΔH>0 4NO2(g)+O2(g) ΔH>0在室温下能自发进行 | 这是一个熵增的反应 |
| B | 压缩针筒内的NO2和N2O4混合气体, 颜色先变深后变浅 | 增大压强,平衡向生成N2O4的方向移动,新平衡比旧平衡压强小 |
| C | 锌与稀硫酸反应过程中,开始反应后速率逐渐增大 | 该反应是放热反应 |
| D | 已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动 | 反应物的浓度一定降低 |
可逆反应N2+3H2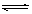 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化表示。下列各关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化表示。下列各关系中能说明反应已达到平衡状态的是
| A.3υ正 (N2)=υ正 (H2) | B.υ正 (N2)=υ逆 (NH3) |
| C.2υ正 (H2)=3υ逆 (NH3) | D.υ正 (N2)=3υ逆 (H2) |
下列不能用勒夏特列原理解释的是
| A.棕红色NO2加压后颜色先变深后变浅 |
| B.冰镇啤酒打开瓶塞后产生大量泡沫 |
| C.在H2,I2(g)和HI组成的平衡体系中加压后,混合物颜色加深 |
| D.Fe(SCN)3溶液中加入固体KSCN后颜色变化 |
一定温度下,向aL密闭容器中加入2mol NO2(g),发生如下反应:2NO2 2NO+O2,此反应达到平衡状态的标志是
| A.混合气体的密度不再变化 |
| B.混合气体的颜色变浅 |
| C.混合气体中NO2、NO、O2的物质的量之比为2:2:1 |
| D.单位时间内生成2n mol NO同时生成2n mol NO2 |
在一定温度下,将气体X和气体Y 各0.16 mol充入10 L恒容密闭容器中,发生反应
X(g) + Y(g)  2Z(g) ?H<0,一段时间后达到平衡,反应过程中测定的数据如下表。下列说法正确的是
2Z(g) ?H<0,一段时间后达到平衡,反应过程中测定的数据如下表。下列说法正确的是
| t / min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10–5 mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大