在一定容积的密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)  2C(g) ΔH<0。达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是 ( )
2C(g) ΔH<0。达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是 ( )
| | X | Y |
| A | 再加入A | B的转化率 |
| B | 加入催化剂 | A的体积分数 |
| C | 充入氦气 | A的转化率 |
| D | 升高温度 | C的体积分数 |
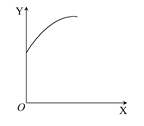
往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)  2HI(g) ΔH<0,当达到平衡后,t0时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是 ( )
2HI(g) ΔH<0,当达到平衡后,t0时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是 ( )
| A.容器内气体颜色变深,平均相对分子质量不变 |
| B.平衡不移动,混合气体密度不变 |
| C.H2转化率增大,HI平衡浓度减小 |
| D.t0时改变的条件是减小体积或升高体系温度 |
将1 mol A2和1 mol B2通入一容积不变的密闭容器中,在一定温度和催化剂作用下,发生反应:2A2(g)+B2(g)  2A2B(g)。反应达到平衡时A2B为0.3 mol。若此时移走0.5 mol A2和0.5 mol B2,则重新达到平衡后,A2B的物质的量( )
2A2B(g)。反应达到平衡时A2B为0.3 mol。若此时移走0.5 mol A2和0.5 mol B2,则重新达到平衡后,A2B的物质的量( )
| A.等于0.3 mol |
| B.等于0.15 mol |
| C.小于0.15 mol |
| D.大于0.15 mol,小于0.3 mol |
下列有关化学平衡图像描述正确的是 ( )
| A.图像A代表任何可逆反应中生成物浓度随温度的变化关系图 |
B.图像B表示反应的化学方程式为:2Z(s)  3X(g)+2Y(g) 3X(g)+2Y(g) |
| C.图像C代表在10 L容器、850℃时反应,到4 min时,反应放出51.6 kJ的热量 |
D.图像D代表等物质的量的气体A和B,在一定温度下发生反应A(g)+xB(g)  2C(g),达到平衡后,只改变反应的一个条件,其在20~40 min之间的平衡常数不相等 2C(g),达到平衡后,只改变反应的一个条件,其在20~40 min之间的平衡常数不相等 |
在一定温度下,反应C(s)+H2O(g)  CO(g)+H2(g)达到平衡的标志是( )
CO(g)+H2(g)达到平衡的标志是( )
| A.正反应与逆反应速率均为零 |
| B.v(H2O生成)=v(CO消耗) |
| C.单位时间内反应物减少的分子数等于生成物增加的分子数 |
| D.压强不随时间的变化而变化 |
在一密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,探讨温度对反应的影响,实验结果如下图所示(注:T1,T2均大于300 ℃),下列说法正确的是 ( )。
A.温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)= mol·L-1·min-1 mol·L-1·min-1 |
| B.该反应在T1时的平衡常数比T2时的小 |
| C.该反应为吸热反应 |
D.处于A点的反应体系从T1变到T2,达到平衡时 增大 增大 |
在我国汽车尾气已成为主要的大气污染物,使用稀土等催化剂能将汽车尾气中的CO、NOx和碳氢化合物转化成无毒物质,从而减少污染。向容积相同的两个密闭容器内(装有等量的某种催化剂),分别充入等量的NOx及C3H6,在不同温度下,发生如下反应: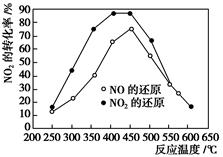
①18 NO(g)+2C3H6(g) 9N2(g)+6CO2(g)+6H2O(g);
9N2(g)+6CO2(g)+6H2O(g);
②18 NO2(g)+4C3H6(g) 9N2(g)+12 CO2(g)+12 H2O(g)
9N2(g)+12 CO2(g)+12 H2O(g)
分别测定不同温度时NOx的转化率,所得的曲线如图所示。下列说法正确的是( )。
| A.该反应的ΔH>0 |
| B.加入催化剂,NO(g)的转化率比NO2(g)的低 |
| C.分离出H2O(g)可提高碳氢化合物的转化率 |
| D.增大C3H6(g)的浓度可提高NOx的转化率,具有实际意义 |
利用醋酸二氨合铜[Cu(NH3)2Ac]溶液吸收CO,能达到保护环境和能源再利用的目的,反应方程式为Cu(NH3)2Ac+CO+NH3 [Cu(NH3)3]Ac·CO。已知该反应的化学平衡常数与温度的关系如表所示:
[Cu(NH3)3]Ac·CO。已知该反应的化学平衡常数与温度的关系如表所示:
| 温度/℃ | 15 | 50 | 100 |
| 化学平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法正确的是 ( )。
A.上述正反应为吸热反应
B.15 ℃时,反应[Cu(NH3)]Ac·CO
 Cu(NH3)2Ac+CO+NH3的平衡常数为0.5
Cu(NH3)2Ac+CO+NH3的平衡常数为0.5C.保持其他条件不变,减小压强,CO的转化率减小
D.醋酸二氨合铜溶液的浓度大小对CO的吸收没有影响
下图是向100 mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图像,根据如图所得结论正确的是 ( )
| A.原来盐酸的物质的量浓度为0.1 mol·L-1 |
| B.NaOH溶液的浓度为0.1 mol·L-1 |
| C.原来盐酸的物质的量浓度为1 mol·L-1 |
| D.NaOH溶液的浓度为0.01 mol·L-1 |