某兴趣小组为探究外界条件对可逆反应A(g)+B(g)  C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1 mol A和1 mol B,反应达平衡时测得容器中各物质的浓度为I。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ。
C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1 mol A和1 mol B,反应达平衡时测得容器中各物质的浓度为I。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ。
| | A | B | C |
| Ⅰ | 0.050 mol·L-1 | 0.050 mol·L-1 | 0.050 mol·L-1 |
| Ⅱ | 0.070 mol·L-1 | 0.070 mol·L-1 | 0.098 mol·L-1 |
| Ⅲ | 0.060 mol·L-1 | 0.060 mol·L-1 | 0.040 mol·L-1 |
| Ⅳ | 0.080 mol·L-1 | 0.080 mol·L-1 | 0.12 mol·L-1 |
针对上述系列试验,下列结论中错误的是 ( )
A.由Ⅰ中数据可计算出该温度下反应的平衡常数K=20 mol-1·L
B.Ⅱ可能是通过增大C的浓度实现的
C.若Ⅲ只是升高温度,则与I比较,可以判断出正反应一定是放热反应
D.第Ⅳ组实验数据的得出,通过压缩容器的体积就可以实现
下图表示反应X(g)+4Y(g)  5Z(g) ΔH<0,在某温度时X的浓度随时间变化的曲线:
5Z(g) ΔH<0,在某温度时X的浓度随时间变化的曲线:
下列有关该反应的描述正确的是 ( )
| A.若Z是有色气体,只压缩容器的体积,平衡不移动,则气体颜色不变 |
| B.若升高温度,则X的平衡转化率减小,v(逆)增大,v(正)减小 |
| C.若X和Y的平衡转化率相等,则起始时X和Y的物质的量之比为1:4 |
| D.若平衡时X的转化率为85%,则起始时Y的物质的量浓度为3.4 mol/L |
COCl2俗名称作光气,是有毒气体。在一定条件下,可发生的化学反应为:COCl2(g)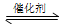 CO(g)+Cl2(g) ΔH<0,下列有关说法不正确的是 ( )
CO(g)+Cl2(g) ΔH<0,下列有关说法不正确的是 ( )
| A.在一定条件下,使用催化剂能加快反应速率 |
| B.当反应达平衡时,恒温恒压条件下通入Ar,COCl2的转化率不变 |
| C.单位时间内生成CO和消耗Cl2的物质的量比为1∶1时,反应达到平衡状态 |
| D.平衡时,其他条件不变,升高温度可使该反应的平衡常数减小 |
在密闭的容器中进行如下反应:H2(g)+I2(g)  2HI(g),在温度T1和T2时,产物的量和时间的关系如图所示,根据图像判断正确的是 ( )
2HI(g),在温度T1和T2时,产物的量和时间的关系如图所示,根据图像判断正确的是 ( )
| A.T1<T2,ΔH<0 | B.T1>T2,ΔH<0 | C.T1<T2,ΔH>0 | D.T1>T2,ΔH>0 |
某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法错误的是
| 物质 | X | Y | Z | W |
| 初始浓度/mol·L-1 | 0.5 | 0.6 | 0 | 0 |
| 平衡浓度/mol·L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
A.反应达到平衡时,X的转化率为80%
B.该反应的平衡常数表达式为K=

C.增大压强其平衡常数不变,但使平衡向生成Z的方向移动
D.改变温度可以改变此反应的平衡常数
在一定温度条件下,对于已达到平衡的反应:
FeCl3 +3KSCN  3KCl+Fe(SCN)3,在此溶液中作如下处理,平衡左移的是
3KCl+Fe(SCN)3,在此溶液中作如下处理,平衡左移的是
| A.加入少量氯化钾固体 | B.加入少量氯化铁固体 |
| C.减少Fe(SCN)3的浓度 | D.加水稀释 |
下列事实不能用勒夏特列原理解释的是 ( )。
| A.氢气和氮气合成氨的反应中,在加压下有利于氨的生成 |
| B.醋酸溶液中滴入少量稀盐酸,溶液中c(H+)增大 |
| C.用热的纯碱水溶液洗涤油污物品时,去污效果较好 |
| D.加催化剂V2O5,能提高SO2转化为SO3的转化率 |
对于可逆反应N2(g)+3H2(g)  2NH3(g);ΔH<0,下列研究目的和示意图相符的是 ( )。
2NH3(g);ΔH<0,下列研究目的和示意图相符的是 ( )。
| | A | B | ||
| 研究 目的 | 压强对反应的影 响(p2>p1) | 温度对反应的影响 | ||
| 图示 | 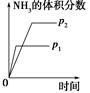 |  | ||
| | C | D | | |
| 研究 目的 | 平衡体系增加N2 对反应的影响 | 催化剂对反应的影响 | | |
| 图示 |  | 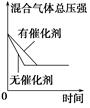 | | |
下列关于平衡常数的说法中,正确的是 ( )。
| A.在平衡常数表达式中,反应物浓度用起始浓度表示,生成物浓度用平衡浓度表示 |
| B.化学平衡常数较大的可逆反应,所有反应物的转化率一定大 |
| C.可以用化学平衡常数来定量描述化学反应的限度 |
| D.平衡常数的大小与温度、浓度、压强、催化剂有关 |