相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)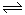 2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表: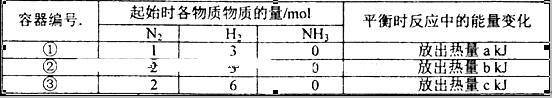
下列叙述正确的是
| A.放出热量关系:a<b <92.4 |
| B.三个容器内反应的平衡常数:③>①>② |
| C.达平衡时氨气的体积分数:①>③ |
| D.N2的转化率:②>①>③ |
为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究。已知:CO2(g)+3H2(g) 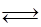 CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。T1℃时,向体积为1L的恒容密闭容器中充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示,且平衡时体系压强为P1。下列叙述中不正确的是
CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。T1℃时,向体积为1L的恒容密闭容器中充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示,且平衡时体系压强为P1。下列叙述中不正确的是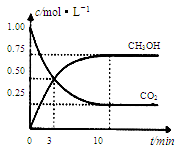
| A.0~3 min内,v(CO2)正 =v (CH3OH)正 |
| B.其他条件不变,若向平衡后的体系中充入1mol氦气,体系压强增大平衡将向正方向移动 |
| C.在T1℃时,若起始时向容器中充入2molCO2和6mol H2 , 测得平衡时容器内压强为P2, 则 P2<2P1 |
| D.T2℃时,上述反应平衡常数为4.2,则T2>T1 |
在一定温度下,容积为2L的密闭容器中x(g).与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图(1)所示;若其他条件不变,温度为T1和T2时,Y的体积分数与时间的关系如图(2)所示。下列说法正确的是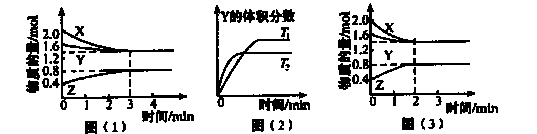
A.容器内发生的反应可以表示为2X(g)+Y(g)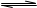 2Z(g) 2Z(g) |
| B.保持其他条件不变,升高温度,该反应的平衡常数K减小 |
| C.反应前3 min内,v(Z)≈0.067 mol·L-1·min-1 |
| D.若改变反应条件,反应进程如图(3)所示,则改变的条件是增大压强 |
 kJ
kJ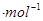 。在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示。下列说法错误的是
。在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示。下列说法错误的是
| A.前25min内反应放出的热量为46.lkJ |
| B.第25min改变的条件是将NH3从反应体系中分离出去 |
| C.若第60min时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
| D.若时段I中投入物质的浓度为原来的2倍,则反应物的转化率增大,平衡常数不变 |
在盛有足量M的体积可变的密闭容器中加入N,发生反应:M (s) +2N (g)==4P (s) +Q (g) ΔH< 0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是
| A.平衡是N的转化率为50% |
| B.当温度升高后,则图中θ>450 |
| C.若再加入N,则正、逆反应速率均逐渐增大 |
| D.若再加入N,则反应体系中气体密度减小 |
对可逆反应4NH3(g)+ 5O2(g)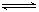 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
| A.达到化学平衡时,υ正=υ逆=0 |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态 |
| C.达到化学平衡时,若增大容器体积,则正反应速率减少,逆反应速率增大 |
| D.达到化学反应平衡后,改变条件当υ正>υ逆,平衡向正反应方向移动 |
从下列实验事实所引起的相应结论不正确的是:
| 选项 | 实 验 事 实 | 结 论 |
| A | 其它条件不变, 0.01mol/L的KMnO4酸性溶液分别与0.1mol/L的H2C2O4溶液和0.2mol/L的H2C2O4溶液反应,后者褪色时间短。 | 当其它条件不变时,增大反应物浓度可以使化学反应速率加快 |
| B | 其它条件不变,分别将等体积、等物质的量浓度的Na2S2O3溶液和H2SO4混合液放在冷水和热水中,放在热水中的混合液先出现浑浊。 | 当其它条件不变时,反应体系的温度越高、化学反应速率越快 |
| C | 将少量MnO2粉末加入盛有10%双氧水的锥形瓶内,在化学反应前后,MnO2的质量和化学性质都没有发生改变。 | 催化剂虽然可以加快化学反应的速率,但一定不参与化学反应过程 |
| D | 一定条件下,分别在容积为1L和容积为2L的两个密闭容器中加入等量的氢气和碘蒸气,发生如下反应:H2(g)+I2(g) 2HI(g),获得等量HI时需要的时间前者少。 2HI(g),获得等量HI时需要的时间前者少。 | 当其它条件不变时,气态反应体系的压强越大、化学反应速率越快 |
下列措施对增大反应速率明显有效的是
| A.在K2SO4与BaCl2两溶液反应时,增大压强 |
| B.Fe与稀硫酸反应制取H2时,改用浓硫酸 |
| C.Na与水反应时增大水的用量 |
| D.Al在氧气中燃烧生成A12O3,将Al片改成Al粉 |
决定化学反应速率的主要因素是
| A.参加反应的物质本身的性质 | B.催化剂 |
| C.温度、压强以及反应物的接触面 | D.反应物的浓度 |
下列叙述表示可逆反应N2 + 3H2 2NH3一定处于平衡状态的是……… ( )
2NH3一定处于平衡状态的是……… ( )
| A.N2、H2、NH3的百分含量相等 | B.3v(N2)正= v(H2)逆 |
| C.定容容器中,气体的密度不变 | D.N2、H2、NH3的浓度之比为1:3:2 |