可逆反应A(?)+a B(g)? ?C(g)+2 D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列说法不正确的是
?C(g)+2 D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列说法不正确的是 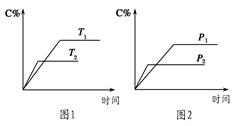
| A.当压强由p1变为 p2时,逆反应速率将变大 |
| B.该反应的正反应为放热反应 |
| C.若a=2,则A为液态或固体 |
| D.恒温恒容条件下,增加B的物质的量,B的转化率和该反应的化学平衡常数都将增大 |
下列有关反应限度的说法错误的是
| A.某条件下可逆反应达到限度之前,逆反应速率逐渐增大可能与生成物浓度逐渐增大有关 |
| B.炼铁高炉尾气中CO含量不随高炉高度改变而改变,是因为有关反应达到了限度 |
| C.化学反应的限度决定了反应物在该条件下的最大转化率 |
| D.可逆反应的限度不随反应条件的改变而改变 |
对于反应2SO2+O2 2SO3下列判断正确的是
2SO3下列判断正确的是
| A.2 mol SO2和足量的O2反应,必生成2 mol SO3 |
| B.平衡时SO2、O2、SO3的分子数之比为2∶1∶2 |
| C.平衡时SO2的消耗速率必定等于O2的生成速率的2倍 |
| D.平衡时SO2的浓度必为O2浓度的2倍 |
决定化学反应速率的根本因素是
| A.温度和压强 | B.反应物的浓度 |
| C.物质自身的性质 | D.催化剂的加入 |
一定温度下,在固定容积的密闭容器中发生下列反应:2HI(g) H2(g)+I2(g)。若HI浓度由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么HI浓度由0.07 mol·L-1降到0.05 mol·L-1时所需反应的时间为
H2(g)+I2(g)。若HI浓度由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么HI浓度由0.07 mol·L-1降到0.05 mol·L-1时所需反应的时间为
| A.等于5 s | B.大于10 s | C.等于10 s | D.小于10 s |
一定温度一定容积下,反应A2(g)+B2(g) 2AB(g)达到平衡的标志是 ( )
2AB(g)达到平衡的标志是 ( )
| A.单位时间内消耗n mol A2同时生成2n mol AB |
| B.容器内的总物质的量不随时间变化 |
| C.单位时间内生成2n mol AB的同时生成n mol B2 |
| D.单位时间内生成n molA2的同时生成n mol B2 |
已知反应4NH3+5O2 4NO+6H2O,若在反应开始后5s~10s之间的反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列判断正确的关系是( )。
4NO+6H2O,若在反应开始后5s~10s之间的反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列判断正确的关系是( )。
A. v(NH3)=v(O2) v(NH3)=v(O2) | B.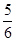 v(O2)=v(H2O) v(O2)=v(H2O) |
C.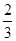 v(NH3)=v(H2O) v(NH3)=v(H2O) | D. v(O2)=v(NO) v(O2)=v(NO) |
某绝热恒容容器中充入2mol/LNO2,发生反应2NO2 N2O4△H=—56.9kJ/mol下列分析不正确的是
N2O4△H=—56.9kJ/mol下列分析不正确的是
| A.5s时NO2的转化率为75% |
| B.0—3s时v(NO2)增大是由于体系温度升高 |
| C.3s时化学反应处于平衡状态 |
| D.9s时再充入N2O4,平衡后K较第一次平衡时大 |
(6分)按要求回答下列问题
(1)把锌片投入到盛有盐酸的敞口容器中,产生H2的速率可由图⑴表示。
在下列因素中对产生H2速率有影响的是 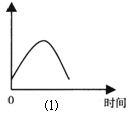
①盐酸的浓度 ②锌片的表面积 ③溶液的温度 ④Cl-的浓度
| A.①④ | B.③④ | C.①②③ | D.②③ |

氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO +3HSO
+3HSO ===3SO
===3SO +Cl-+3H+,已知该反应的速率随溶液酸性的增强而加快。上图为用ClO
+Cl-+3H+,已知该反应的速率随溶液酸性的增强而加快。上图为用ClO 在单位时间内的物质的量浓度的变化来表示该反应的速率一时间图象。下列说法不正确的是( )
在单位时间内的物质的量浓度的变化来表示该反应的速率一时间图象。下列说法不正确的是( )
| A.反应开始时速率增大可能是c(H+)增大引起的 |
| B.纵坐标为v(H+)的速率—时间曲线与图中曲线能完全重合 |
| C.后期反应速率下降的主要原因是反应物的浓度减小 |
| D.图中的阴影部分“面积”为t1~t2时间内ClO的物质的量浓度的减小值 |