在密闭容器中存在下列平衡:CO(g)+H2O(g)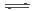 CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如右图所示。下列说法错误的是
CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如右图所示。下列说法错误的是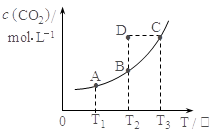
| A.平衡状态A与C相比,平衡状态A的c(CO)小 |
| B.在T2时,若反应处于状态D,则一定有V正<V逆 |
C.反应CO(g)+H2O(g)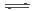 CO2(g)+H2(g) 的ΔH>0 CO2(g)+H2(g) 的ΔH>0 |
| D.若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
下列说法不正确的是
| A.在自然界中存在的单质,一定具备化学性质稳定、不与其它物质发生反应这一特征 |
| B.100多年前,英国曾耗巨资改建高炉,试图延长CO和Fe2O3的接触时间,以减少CO的排放,这违背了化学反应都有一定限度这一基本原理 |
| C.在溶液中,有色物质参与的反应,可以用分光光度计来测定其化学反应速率 |
| D.虽然碳酸钙分解需要吸收大量的热,但在高温条件下也能自发进行 |
一定条件下,向容积为2L的密闭容器中充入l mol CO2和3 molH2,发生如下反应: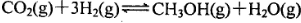 ,5 min后反应达到平衡时c(CH3OH)为0.2 mol
,5 min后反应达到平衡时c(CH3OH)为0.2 mol 。CO2(g)的平衡物质的量浓度c(CO2)与温度关系如图所示。下列说法错误的是
。CO2(g)的平衡物质的量浓度c(CO2)与温度关系如图所示。下列说法错误的是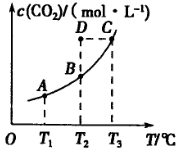
A. 0~5 min,CO2的平均反应速率为0.04 mol.(L.min)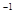 |
B.反应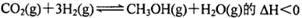 |
C.在T2℃时,若反应处于状态D,则一定有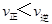 |
| D.若T1℃、T2℃时的平衡常数分别为K1、K2,则K1>K2 |
已知图①~④的相关信息,下列相应叙述正确的是 ( )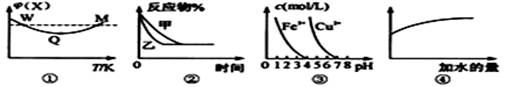
A.图①表示向恒容密闭容器中充入X和Y发生反应:2X(g)+Y(g)  3Z(g) △H﹤0,W点X的正反应速率等于M点X的正反应速率 3Z(g) △H﹤0,W点X的正反应速率等于M点X的正反应速率 |
B.图②表示压强对可逆反应A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强小 3C(g)+D(s)的影响,乙的压强比甲的压强小 |
| C.据图③,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至PH在4左右 |
| D.常温下,稀释0.1mol/LNa2CO3溶液,图④中的纵坐标可表示溶液中HCO3-的数目 |
己知: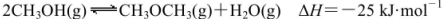 。某温度下的平衡常数为400。此温度下,在1L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如表,下列说法中不正确的是
。某温度下的平衡常数为400。此温度下,在1L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如表,下列说法中不正确的是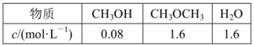
| A.此时刻反应达到平衡状态 |
| B.容器内压强不变时,说明反应达平衡状态 |
| C.平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率不变 |
| D.平衡时,反应混合物的总能量降低40 kJ |
为探究锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是
| A.加入NH4HSO4固体,v(H2)增大 | B.加入少量水,v(H2)不变 |
| C.加入CH3COONa固体,v(H2)减小 | D.滴加少量CuSO4溶液,v(H2)减小 |
把下列四种x的溶液,分别加入盛有10 mL、2 mol/L的盐酸的烧杯中,并均加水稀释至50mL,此时x和盐酸缓和地进行反应,其中反应速率最大的是:
| A.20 mL,2 mol/L | B.20 mL,3 mol/L | C.10 mL,5 mol/L | D.10 mL,3 mol/L |
常温下,0.2 mol·L-1的盐酸30mL分别与下列Na2CO3溶液混合,再加水稀释到100mL,其中最初产生CO2的速率最快的是
| A.20mL0.3 mol·L-1Na2CO3 | B.10mL0.4 mol·L-1Na2CO3 |
| C.25mL0.4 mol·L-1Na2CO3 | D.15mL0.5 mol·L-1Na2CO3 |
 2AB(g) ,反应达到平衡状态的标志是
2AB(g) ,反应达到平衡状态的标志是  2CO(g)反应中可使反应速率增大的措施是
2CO(g)反应中可使反应速率增大的措施是