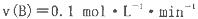在密闭容器中发生反应: aX(g)+bY(g) 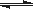 cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述正确的是( )
cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述正确的是( )
| A.平衡向正反应方向移动 | B.(a+b)>(c+d) |
| C.Z的体积分数变大 | D.X的转化率变小 |
设C+CO2 2CO(正反应吸热),正反应的反应速率为v1;N2+3H2
2CO(正反应吸热),正反应的反应速率为v1;N2+3H2 2NH3(正反应放热),正反应的反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为
2NH3(正反应放热),正反应的反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为
| A.v1减小,v2增大 | B.同时减小 |
| C.v1增大,v2减小 | D.同时增大 |
下列物质都能与金属钠反应放出H2,产生H2的速率排序正确的是
①C2H5OH ②NaOH溶液 ③醋酸溶液
| A.③﹥②﹥① | B.②﹥①﹥③ | C.①﹥②﹥③ | D.③﹥①﹥② |
下列有关化学反应速率的说法中,正确的是
A.往容积一定的容器中再通入O2,可以加快反应2SO2+O2 2SO3的反应速率 2SO3的反应速率 |
| B.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 |
C.对于C(s)+H2O(g)  CO(g)+H2(g)的反应,加入固体炭,反应速率加快 CO(g)+H2(g)的反应,加入固体炭,反应速率加快 |
| D.100 mL 2 mol·L-1的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
下列对“化学反应速率”的理解正确的是
| A.化学反应速率表示的是化学反应进行的限度 |
| B.化学反应速率可以用单位时间内反应物浓度的减少量来表示 |
| C.对于任何化学反应来说,反应速率越快,反应现象就越明显 |
| D.化学反应速率可以是正值,也可以是负值 |
反应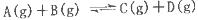 过程中的能量变化如图所示,下列说法错误的是
过程中的能量变化如图所示,下列说法错误的是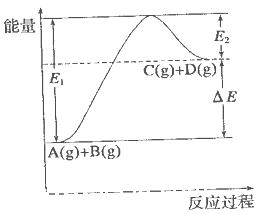
| A.该反应是吸热反应 |
| B.加入催化剂后,反应加快,A的转化率不变 |
| C.反应物的总键能小于生成物的总键能 |
| D.反应达到平衡时,升高温度,A的转化率增大 |
700℃时,向容积为1 L的密闭容器中充入一定量的CO2和H2,发生反应:
CO2+H2(g)  CO(g)+H2O(g) 反应过程中测定的部分数据见下表(表中t2>t1):
CO(g)+H2O(g) 反应过程中测定的部分数据见下表(表中t2>t1):
| 反应时间/min | n(CO2)/mol | H2/ mol |
| 0 | 1.50 | 1.00 |
| t1 | | 0.40 |
| t2 | 0.90 | |
A.反应在t1 min内的平均速率为v(H2O)=0.60 /t1 mol·L-1·min-1
B.温度升至800℃,上述反应平衡常数为1.56,则正反应为放热反应
C.保持其他条件不变,向平衡体系中再通入1.00 molH2,与原平衡相比,达到新平时CO2转化率增大,H2的体积分数增大
D.保持其他条件不变,起始时向容器中充入1.00 molCO和1.50 molH2O,到达平衡时,c(CO2)=0.90 mol/L
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示。
下列说法不正确的是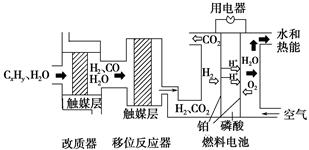
| A.该系统中只存在化学能和电能的相互转化 |
B.在移位反应器中,反应CO(g)+H2O(g) 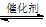 CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大 CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大 |
| C.改质器和移位反应器的作用是将CxHy转化为H2和CO2 |
| D.该电池正极的电极反应为O2+4H++4e-=2H2O |
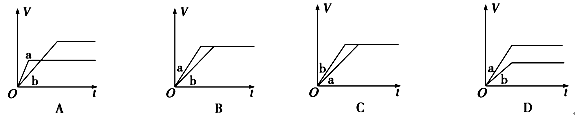
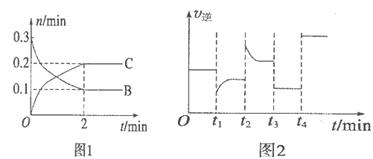
 B、C的物质的量随时间变化的关系如图l,达平衡后在
B、C的物质的量随时间变化的关系如图l,达平衡后在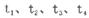 时都只改变了一种条件,逆反应速率随时间变化的关系如图2。下列有关说法正确的是
时都只改变了一种条件,逆反应速率随时间变化的关系如图2。下列有关说法正确的是