一定条件下存在反应:CO(g)+H2O(g)?CO2(g)+H2(g),其正反应放热.现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol CO和1mol H2O,在Ⅱ中充入1mol CO2和1mol H2,在Ⅲ中充入2mol CO 和2mol H2O,700℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A.容器Ⅰ中CO 的物质的量比容器Ⅱ中的多 |
| B.容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C.容器Ⅰ、Ⅱ中正反应速率相同 |
| D.容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和等于1 |
下列事实不能用勒夏特列原理解释的是 ( )
| A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
| B.合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率; |
| C.过氧化氢分解加二氧化锰作催化剂,使单位时间内产生的氧气的量多。 |
| D.久制的氯水PH值变小。 |
化学与科学、技术、社会和环境密切相关。下列说法正确的是( )
| A.化学平衡常数是指一定条件下的可逆反应,生成物浓度的幂之积与反应物浓度的幂之积的比值。 |
| B.已知4HCl(g)+O2(g)=2H2O(g)+2Cl2(g) 能自发进行,则该反应ΔH<0,ΔS>0 |
| C.其他条件不变,增大压强,平衡可能移动,但平衡常数一定不变 |
| D.铁制品表面镶锌块和铁制品表面镀锡,都能起到防腐的作用且防腐原理是相同的 |
可以充分说明反应P(g)+Q(g) R(g)+S(g)在恒温下已达到平衡的是( )
R(g)+S(g)在恒温下已达到平衡的是( )
| A.反应容器内的压强不随时间改变 | B.反应容器内P、Q、R、S四者共存 |
| C.P的生成速率和S的生成速率相等 | D.反应容器内的气体总物质的量不随时间变化 |
T ℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z 的 浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论错误的是
A.容器中发生的反应可表示为:3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.反应进行前3min内,用X表示的反应速率v(X)=0.1mol/(L·min) |
| C.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
| D.保持其他条件不变,升高温度,化学平衡向逆反应方向移动 |
下列叙述中一定能判断某化学平衡发生移动的是( )
| A.混合物中各组分的浓度改变 | B.正、逆反应速率改变 |
| C.混合物中各组分的含量改变 | D.混合体系的压强发生改变 |
 2CO(g)△H>0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;
2CO(g)△H>0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;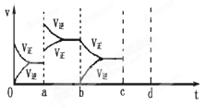
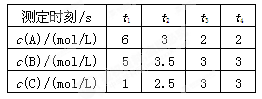
 2C
2C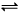 2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是
2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是