题目内容
在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4时刻测得各物质的浓度如下表.据此判断下列结论正确的是( )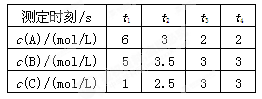
A.在t3时刻反应已经停止
B.A的转化率比B的转化率低
C.在t2~t3内A的平均反应速率为: [1/(t3-t2)]mol/(L·s)
D.在容器中发生的反应为:2A+B 2C
2C
C
解析

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
用下列方法制取氢气,反应速率最大的是
| A.10℃时,粉末状锌与2 mol·L-1硫酸溶液反应 |
| B.30℃时,粉末状锌与2mol·L-1硫酸溶液反应 |
| C.10℃时,块状锌与2 mol·L-1硫酸溶液反应 |
| D.30℃时,块状锌与2 mol·L-1硫酸溶液反应 |
溴水中存在着如下的平衡:Br2+H2O HBr+HBrO,下列措施,不能使溶液颜色变浅的是
HBr+HBrO,下列措施,不能使溶液颜色变浅的是
| A.通入乙烯气体 | B.通入SO2气体 | C.加入NaF晶体 | D.加入NaI晶体 |
下列关于化学反应的速率和限度的说法不正确的是( )
| A.任何可逆反应都有一定的限度 |
| B.影响化学反应速率的条件有温度、催化剂、浓度等 |
| C.化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| D.决定反应速率的主要因素是反应物的性质 |
在恒容密闭容器中,由CO合成甲醇:CO(g) + 2H2(g)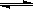 CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如右图所示,下列说法正确的是
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如右图所示,下列说法正确的是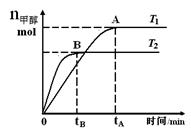
A.平衡常数K = 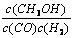 |
| B.该反应在T1时的平衡常数比T2时的小 |
| C.任意时刻,T2温度下的反应速率均大于T1温度下的速率 |
D.处于A点的反应体系从T1变到T2,达到平衡时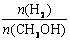 增大 增大 |
对于可逆反应4NH3+5O2 4NO+6H2O(g),下列叙述不正确的是 ( )
4NO+6H2O(g),下列叙述不正确的是 ( )
| A.达到平衡时,4v(O2)正=5v(NO)逆 |
| B.达到平衡状态后,NH3、O2、NO 、H2O(g)的物质的量保持不变。 |
| C.达到平衡状态时,若增加容器体积,则反应速率增大 |
| D.若单位时间生成xmolNO的同时,生成xmolNH3,则反应达到平衡状态 |
一定条件下存在反应:CO(g)+H2O(g)?CO2(g)+H2(g),其正反应放热.现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol CO和1mol H2O,在Ⅱ中充入1mol CO2和1mol H2,在Ⅲ中充入2mol CO 和2mol H2O,700℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A.容器Ⅰ中CO 的物质的量比容器Ⅱ中的多 |
| B.容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C.容器Ⅰ、Ⅱ中正反应速率相同 |
| D.容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和等于1 |
 2C(g) △H<0,下列各图正确的是( )
2C(g) △H<0,下列各图正确的是( )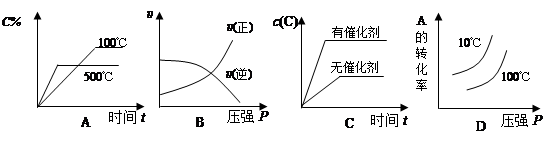
 2C(气)达到平衡的标志是( )
2C(气)达到平衡的标志是( )