t℃时,在体积不变的容器中发生反应X(g)+3Y(g) 2Z(g)△H<O各组分浓度如下表
2Z(g)△H<O各组分浓度如下表
| 物质 | X | Y | Z |
| 初始浓度/ mol·L-1 | 0.1 | 0.3 | 0 |
| 2min末浓度/mol·L-1 | 0.08 | | |
| 平衡浓度/mol·L-1 | | | 0.1 |
A .0~2min的平均速率v(x) ="0." 01 mol·L-1·min-1
B.达平衡时Y的转化率为50%
C.其它条件不变,升高温度,平衡逆向移动
D.其它条件不变,增加X的浓度,ν正增大
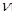 逆碱小,平衡正向移动
逆碱小,平衡正向移动 在可逆反应2SO2+O2 2SO3中,充入一定量的18O2,足够长的时间后,18O原子
2SO3中,充入一定量的18O2,足够长的时间后,18O原子
| A.只存在于O2中 | B.只存在于O2和SO3中 |
| C.只存在于O2和SO2中 | D.存在于O2、SO2和SO3中 |
把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是
| A.盐酸的浓度 | B.铝条的表面积 | C.溶液的温度 | D.加少量Na2SO4固体 |
决定化学反应速率的主要因素是
| A.催化剂 | B.参加反应的物质本身的性质 |
| C.反应物的浓度 | D.温度、压强以及反应物的接触面 |
已知反应A2(g)+2B2(g) 2AB2(g)△H <0,下列说法正确的
2AB2(g)△H <0,下列说法正确的
| A.升高温度,正向反应速率增加,逆向反应速率减小 |
| B.升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
影响化学反应速率与平衡的因素有多方面,如浓度压强温度催化剂等。下列有关说法不正确的是
| A.其它条件不变时,改变压强能改变气体反应的速率,但不一定改变平衡 |
| B.增大浓度能加快化学反应速率,原因是增大浓度就增加了反应体系中活化分子的百分数 |
| C.温度升高使化学反应速率加快的主要原因是增加了反应体系中活化分子的百分数 |
| D.加入催化剂能降低反应所需的活化能,使反应速率加快,平衡常数增大 |
mA(s)+nB(g)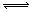 qC(g)的可逆反应中,图甲在恒温条件达平衡时,B的体积分数(B%)与压强(p)的关系,图乙表示在一定条件下达到平衡(v正=v逆)后t1时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,有关叙述正确的是
qC(g)的可逆反应中,图甲在恒温条件达平衡时,B的体积分数(B%)与压强(p)的关系,图乙表示在一定条件下达到平衡(v正=v逆)后t1时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,有关叙述正确的是
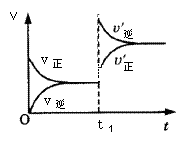
甲 乙
| A.n<q | B.n>q |
| C.正反应为放热反应 | D.X点比Y点反应速率快 |
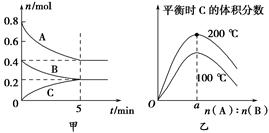
 zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )。
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )。