下列反应属于吸热反应的是 ( )
| A.中和反应 | B.锌与稀硫酸反应 |
| C.炭燃烧生成CO | D.炭与高温水蒸汽反应 |
合理利用燃料减小污染符合“绿色奥运”理念,下列关于燃料的说法正确的是( )
| A.“可燃冰”是将水变为油的新型燃料 |
| B.氢气是具有热值高、无污染等优点的燃料 |
| C.乙醇是比汽油更环保、不可再生的燃料 |
| D.石油和煤是工厂经常使用的可再生的化石燃料] |
白磷与氧可发生如下反应:P4+5O2= P4O10。已知断裂下列化学键需要吸收的能量分别为: P-P:a kJ·mol-1、P-O:b kJ·mol-1、P=O:c kJ·mol-1、O=O:d kJ·mol-1,根据图示的分子结构和有关数据估算该反应的 H,其中正确的是( )
H,其中正确的是( )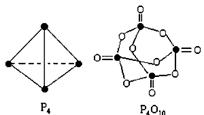
| A.(6a+5d-4c-12b) kJ·mol-1 | B.(4c+12b-6a-5d) kJ·mol-1 |
| C.(4c+12b-4a-5d) kJ·mol-1 | D.(4a+5d-4c-12b) kJ·mol-1 |
科学家正在研究开发新的能源,如核能、太阳能、风能、地热、潮汐热等。“绿色能源”是目前正在研究的新能源之一,把高粱、玉米等绿色植物的种子经发酵、蒸馏就可以得到“绿色能源”中的一种。这种物质是( )
| A.氢气 | B.甲烷 | C.酒精 | D.木炭 |
单斜硫和正交硫是硫的两种同素异形体。已知
①S(s,单斜)+O2(g)=SO2(g) ΔH1=-297.16 kJ/mol
②S(s,正交)+O2(g)=SO2(g) ΔH2=-296.83 kJ/mol
下列说法正确的是( )
| A.正交硫比单斜硫稳定 |
| B.S(s,单斜)=S(s,正交)ΔH3=+0.33 kJ/mol |
| C.相同物质的量的正交硫比单斜硫所含有的能量高 |
| D.①式表示断裂1 mol O2中的共价键所吸收的能量比形成1 mol SO2中的共价键所放出的能量多297.16 kJ |
下列说法正确的组合是( )
(1)放热反应不需要加热就能反应,吸热反应不加热就不能反应
(2)物质发生化学变化都伴有能量的变化
(3)伴有能量变化的物质变化都是化学变化
(4)吸热反应和放热反应都有可能自发进行
(5)Na转化为Na+时,吸收的能量就是该过程的反应热
(6)水蒸气变为液态水时放出的能量就是该变化的反应热
| A.(1)(2) | B.(3)(5) | C.(2)(6) | D.(2)(4) |
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(1) △H=-57.3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应△H1、△H2、△H3的关系正确的是
| A.△H1>△H2>△H3 | B.△H1<△H3<△H2 | C.△H1<△H2<△H3 | D.△H1>△H3>△H2 |
工业生产水煤气的反应为:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.4 kJ/mol,下列判断正确的是( )
| A.反应物能量总和小于生成物能量总和 |
| B.CO(g)+H2(g)=C(s)+H2O(g) ΔH=+131.4 kJ/mol |
| C.水煤气反应中,生成1 mol H2(g)吸收131.4 kJ热量 |
| D.水煤气反应中生成1体积CO(g)吸收131.4 kJ热量 |
已知下列反应的热化学方程式为
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
(2)C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ/mol
(3)H2(g)+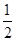 O2(g)=H2O(l) ΔH3=-285.8 kJ/mol
O2(g)=H2O(l) ΔH3=-285.8 kJ/mol
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的ΔH为( )
| A.-488.3 kJ/mol | B.-191 kJ/mol | C.-476.8 kJ/mol | D.-1 549.6 kJ/mol |
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2 800 kJ/mol,则下列热化学方程式正确的是 ( )
A.C(s)+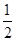 O2(g)=CO(g) ΔH=-393.5 kJ/mol O2(g)=CO(g) ΔH=-393.5 kJ/mol |
| B.2H2(g)+O2(g)=2H2O(g) ΔH=+571.6 kJ/mol |
C.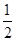 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)ΔH=-1 400 kJ/mol C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)ΔH=-1 400 kJ/mol |
| D.CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-890.3 kJ/mol |