已知:H+(aq) + OH—(aq)=H2O(l) △H=—57.3kJ/mol。向1L 0.5mol/L的NaOH溶液中加入下列物质:①稀盐酸;②浓H2SO4;③稀醋酸,恰好完全反应的热效应△H1、△H2、△H3的关系正确的是
| A.△H1>△H2>△H3 | B.△H3>△H1>△H2 |
| C.△H1=△H3>△H2 | D.△H2>△H1>△H3 |
下列热化学方程式正确的是(△H的绝对值均正确)( )
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0kJ·mol-1(燃烧热) |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)ΔH=+57.3kJ·mol-1(中和热) |
| C.S(s)+O2(g)=SO2(g)ΔH=-269.8kJ·mol-1(反应热) |
| D.2NO2=2NO+O2ΔH=+116.2kJ·mol-1(反应热) |
已知反应X+Y=M+N 为放热反应,对该反应的下列说法中正确的是( )
| A.X的能量一定高于M |
| B.Y的能量一定高于N |
| C.X和Y的总能量一定高于M和N的总能量 |
| D.因该反应为放热反应,故不必加热就可发生 |
下列依据热化学方程式得出的结论正确的是( )
A.已知2SO2(g)+O2 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
| B.已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C.已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则任何酸碱中和的反应热均为57.3kJ |
| D.已知2C(s)+2O2(g)=2CO2(g)△H1 |
下列说法正确的是( )
| A.反应热就是反应中放出的热量 |
| B.放热反应的△H>0,吸热反应的△H<0 |
| C.一个化学反应中,当反应物的总能量大于生成物的总能量时,反应放热,△H为“—” |
| D.一个化学反应中,生成物的总键能大于反应物的总键能时,反应吸热,△H为“+” |
根据下列热化学方程式:
(1)C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
(2)H2(g)+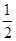 O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
(3)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH3=-870.3 kJ·mol-1
可以计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为 ( )
| A.ΔH=+244.1 kJ·mol-1 |
| B.ΔH=-488.3 kJ·mol-1 |
| C.ΔH=-996.6 kJ·mol-1 |
| D.ΔH=+996.6 kJ·mol-1 |
已知下列热化学方程式:
Zn(s)+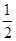 O2(g)=ZnO(s) ΔH1=-351.1 kJ·mol-1
O2(g)=ZnO(s) ΔH1=-351.1 kJ·mol-1
Hg(l)+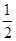 O2(g)=HgO(s) ΔH2=-90.7 kJ·mol-1
O2(g)=HgO(s) ΔH2=-90.7 kJ·mol-1
由此可知Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH3,其中ΔH3的值是 ( )
| A.-441.8 kJ·mol-1 | B.-254.6 kJ·mol-1 |
| C.-438.9 kJ·mol-1 | D.-260.4 kJ·mol-1 |
强酸与强碱在稀溶液中发生中和反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,向3份同体积0.2 mol ·L-1的NaOH溶液中分别加入适量的稀醋酸、浓硫酸、稀硝酸,恰好完全反应的热效应ΔH1、ΔH2、ΔH3的关系正确的是 ( )
| A.ΔH1>ΔH2>ΔH3 | B.ΔH2>ΔH3>ΔH1 |
| C.ΔH2>ΔH1>ΔH3 | D.ΔH1>ΔH3>ΔH2 |

