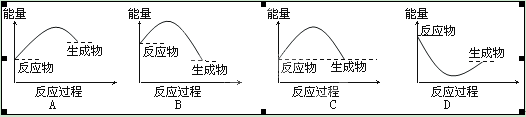
下列说法中,正确的是
| A.放热反应不需要加热就可以发生 |
| B.化学反应除了生成新物质外,还伴随着能量的变化 |
| C.反应条件为加热的反应都是吸热反应 |
| D.化学反应放热还是吸热,取决于反应条件 |
分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是
| “嫦娥一号” 发射火箭燃料 | 液氢(H2) | ①2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1 ②2H2(l)+O2(l)=2H2O(g) △H=-482.6kJ·mol-1 |
| 北京奥运会“祥云” 火炬燃料 | 丙烷(C3H8) | ③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g)△H=-2013.8kJ·mol-1 ④C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2221.5kJ·mol-1 |
C.285.8 kJ·mol-1,2013.8 kJ·mol-1 D.285.8 kJ·mol-1,2221.5 kJ·mol-1
碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
①H2(g) + I2(?) 2HI(g)+9.48kJ
2HI(g)+9.48kJ
②H2(g) + I2(?) 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判断正确的是
| A.①中的I2为固态,②中的I2为气态 |
| B.②的反应物总能量比①的反应物总能量低 |
| C.①的产物比反应②的产物热稳定性更好 |
| D.1mol 固态碘升华时将吸热17kJ |
氢化热是指一定条件下,1 mol 不饱和化合物加氢时放出的热量。表中是环己烯( )、环己二烯(
)、环己二烯( )和苯的氢化热数据。
)和苯的氢化热数据。
| 化合物 | 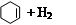  | 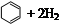  | 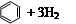  |
| 氢化热 (kJ/mol) | 119.7 | 232.7 | 208.4 |
根据表中数据推断正确的是
A.环己二烯与H2的反应最剧烈
B.环己烯、环己二烯和苯有相同的官能团
C.三种化合物中环己二烯的稳定性最强
D.上述条件下,1 mol
 转变为
转变为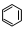 时放热
时放热 与图像有关的叙述,正确的是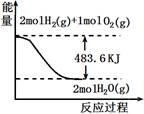
| A.表示1mol H2 (g)完全燃烧生成水蒸气吸收241.8 kJ热量 |
| B.表示的热化学方程式为:H2(g)+ 1/2 O2(g) → H2O(g) +241.8 kJ |
| C.表示2 mol H2(g)所具有的能量一定比2 mol气态水所具有的能量多483.6 kJ |
| D.H2O(g)的能量低于H2(g)和O2(g)的能量之和 |
下列说法正确的是
| A.氢气是一种高效而没有污染的一级能源 |
| B.太阳能、氢能、风能、海洋能、地热能和生物质能等都是新能源 |
| C.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0 |
| D.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。对该反应的有关叙述正确的是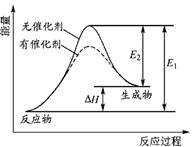
| A.该反应的正反应为吸热反应 |
| B.催化剂能改变反应的焓变 |
| C.催化剂不能降低反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |
已知在1×105Pa,298K条件下,1mol氢气燃烧生成水蒸气放出242kJ热量,下列热化学方程式正确的是
| A.H2(g)+1/2O2(g)=H2O(g) ΔH=+242kJ·mol-1 |
| B.H2O(g)=H2(g)+1/2O2(g) ΔH=+242kJ·mol-1 |
| C.2H2(g)+O2(g)=2H2O(l)ΔH=-484kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g)ΔH=+484kJ·mol-1 |
下列有关热化学方程式的叙述中,正确的是
| A.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为NaOH(aq)+HCl(aq)=NaC1(aq)+H2O(1) ΔH=+57.4kJ/mo1 |
| B.已知C(石墨,s)=C(金刚石,s) ΔH>0,则石墨比金刚石稳定 |
| C.已知2H2(g)+O2(g)=2H2O(g) ΔH =—483.6kJ/mol,则H2燃烧热为241.8kJ/mol |
| D.己知2C(s)+2O2(g)=2CO2(g) ΔH 1;2C(s)+O2(g)="2CO(g)" ΔH 2;则ΔH 1<ΔH 2 |