在298 K、100 kPa时,已知:
2H2O(g)=O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)=2HCl(g) ΔH2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是 ( )。
| A.ΔH3=ΔH1+2ΔH2 | B.ΔH3=ΔH1+ΔH2 |
| C.ΔH3=ΔH1-2ΔH2 | D.ΔH3=ΔH1-ΔH2 |
已知一定条件下断裂1 mol下列化学键生成气态原子需要吸收的能量如下:H—H 436 kJ;Cl—Cl 243 kJ;H—Cl 431 kJ。下列所得热化学方程式或结论正确的是 ( )。
| A.2HCl(g)=H2(g)+Cl2(g)的反应热ΔH<0 |
| B.H(g)+Cl(g)=HCl(g) ΔH=+431 kJ·mol-1 |
| C.相同条件下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相等 |
| D.H2(g)+Cl2(g)=2HCl(g) ΔH=-183 kJ |
下列说法或表示方法正确的是 ( )。
| A.反应物的总能量低于生成物的总能量时,反应一定不能自发进行 |
| B.已知:H2S(g)+aO2(g)=x+bH2O(l) ΔH,若ΔH表示H2S的燃烧热,则x为SO2(g) |
| C.已知:2SO2(g)+O2(g)??2SO3(g) ΔH=-98.3 kJ·mol-1,在密闭容器中充入1 mol SO2和0.5 mol O2,充分反应后放出49.15 kJ的热量 |
| D.由石墨比金刚石稳定可得:C(s,金刚石)=C(s,石墨) ΔH>0 |
已知25 ℃、101 kPa时,1 mol H2与溴蒸气完全反应生成气态溴化氢放出能量Q kJ,则下列热化学方程式书写正确的是 ( )。
| A.H2(g)+Br2(g)=2HBr(g) ΔH=-2Q kJ·mol-1 |
| B.H2(g)+Br2(l)=2HBr(g) ΔH=-Q kJ·mol-1 |
C.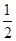 H2(g)+ H2(g)+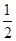 Br2(g)=HBr(g)ΔH=+ Br2(g)=HBr(g)ΔH=+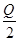 kJ·mol-1 kJ·mol-1 |
D.HBr(g)=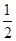 H2(g)+ H2(g)+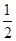 Br2(g)ΔH=+ Br2(g)ΔH=+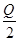 kJ·mol-1 kJ·mol-1 |
“低碳经济”是以低能耗、低污染、低排放为基础的可持续发展的经济模式。下列说法与“低碳经济”不符合的是 ( )。
| A.采用压缩天然气代替燃油 |
| B.加快化石燃料的开采与使用,提高人们的生活水平 |
| C.利用硅材料制成光伏发电装置发电 |
| D.利用太阳能、风能等,减少化石燃料的使用 |
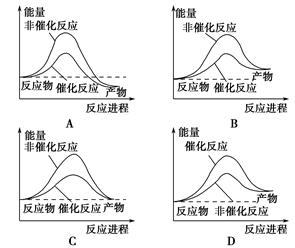
下图是N2与H2反应生成NH3的过程中能量变化的曲线图:下列叙述正确的是( )。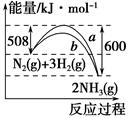
| A.该反应的热化学方程式为 N2(g)+3H2(g)=2NH3(g) ΔH=-92 kJ |
| B.b曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热减小 |
| D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1 |
100 g炭粉燃烧所得气体中,CO占 、CO2占
、CO2占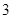 ,且C(s)+
,且C(s)+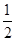 O2(g)=CO(g) ΔH=-110.35 kJ·mol-1,CO(g)+
O2(g)=CO(g) ΔH=-110.35 kJ·mol-1,CO(g)+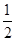 O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1,与这些炭粉完全燃烧相比损失的热量是 ( )。
O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1,与这些炭粉完全燃烧相比损失的热量是 ( )。
| A.784.92 kJ | B.2 489.44 kJ | C.1 569.83 kJ | D.3 274.3 kJ |
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) ΔH1
2H2(g)+O2(g)=2H2O(g) ΔH2
C(s)+O2(g)=CO2(g) ΔH3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为( )。
| A.12ΔH3+5ΔH2-2ΔH1 | B.2ΔH1-5ΔH2-12ΔH3 |
| C.12ΔH3-5ΔH2-2ΔH1 | D.ΔH1-5ΔH2-12ΔH3 |