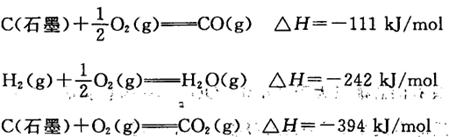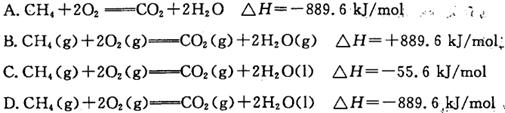下列与化学反应能量变化相关的叙述正确的是 ( )。
| A.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| B.1 mol S完全燃烧放热297.3 kJ,其热化学方程式:S+O2=SO2 ΔH=-297.3 kJ·mol-1 |
| C.1 mol H2SO4与1 mol Ba(OH)2反应生成1 mol BaSO4沉淀时放出的热量叫做中和热 |
| D.反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
下列图示与对应的叙述相符的是( )。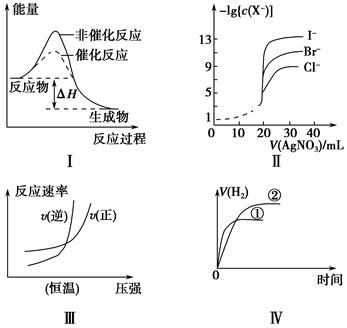
| A.图Ⅰ中ΔH表示某一反应有无催化剂的反应热相同 |
| B.用0.010 0 mol·L-1硝酸银标准溶液,滴定浓度均为0.100 0 mol·L-1 Cl-、Br-及I-的混合溶液,由图Ⅱ曲线,可确定首先沉淀的是Cl- |
| C.图Ⅲ可表示工业合成氨反应在温度一定的情况下反应速率与压强的关系 |
| D.图Ⅳ表示相同体积、相同pH的一元强酸溶液①和一元弱酸溶液②分别与足量的锌粉发生反应,V(H2)随时间的变化曲线 |
如图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1,下列说法或表示式正确的是( )
| A.C(s、石墨)=C(s、金刚石)ΔH=+1.9 kJ·mol-1 |
| B.石墨和金刚石的转化是物理变化 |
| C.金刚石的稳定性强于石墨 |
| D.1 mol石墨的能量比1 mol金刚石的总能量大 |
已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(g) ΔH1=a kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH2=b kJ·mol-1
③H2(g)+1/2O2(g)=H2O(l) ΔH3=c kJ·mol-1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol-1
下列关系式中正确的是( )
| A.a<c<0 | B.b>d>0 |
| C.2a=b<0 | D.2c=d>0 |
下列反应属于放热反应的是( )
①稀硫酸与氢氧化钾溶液反应
②锌与稀硫酸的反应
③生石灰变成熟石灰的反应
④氢氧化钡晶体和氯化铵晶体混合反应
⑤石灰石高温煅烧
⑥灼热的炭与CO2反应
⑦甲烷与O2的燃烧反应
| A.①②③⑤ | B.①②③⑦ |
| C.①②⑤⑥⑦ | D.④⑥ |
下列热化学方程式书写正确的是( )
| A.C(s)+O2(g)=CO2(g)ΔH=+393.5 kJ/mol |
| B.2SO+O2=2SO3ΔH=-196.6 kJ/mol |
| C.H2(g)+1/2O2(g)=H2O(l)ΔH=-285.8 kJ/mol |
| D.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ |
已知下列热化学方程式:Zn(s) + 1/2 O2(g)= ZnO(s) △H1;Hg(l) + 1/2 O2(g)=HgO(s) △H2;
则 Zn(s)+ HgO(s)=Hg(l)+ ZnO(s),△H值为
| A.△H2-△H1 | B.△H2+△H1 | C.△H1-△H2 | D.-△H1-△H2 |
化学与生活、生产息息相关,下列说法不正确的是
| A.煤、石油、天然气属于化石能源,太阳能、氢能、风能、地热能、海洋能属于新能源 |
| B.测试和调控溶液的pH对工农业生产、科学研究及日常生活和医疗保健都有重要意义 |
| C.利用盐类的水解反应可以制备胶体对饮用水进行净化,也可以获得纳米材料 |
| D.通常条件下能够自发进行的反应必须具备△H和△S均小于零 |