在一定条件下A与B反应可生成C和D,其能量变化如图:
下列有关反应A+B=C+D的说法正确的是 ( )。
| A.反应前后原子的种类和数目一定不变 |
| B.反应前后分子的种类和数目一定改变 |
| C.反应物的总能量E1与生成物的总能量E2一定相等 |
| D.此反应一定有热量的变化 |
下列图示与对应的叙述相符的是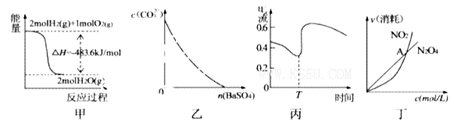
A.图甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483. 6kJ |
| B.图乙表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化 |
| C.图丙表示Zn、Cu和稀硫酸构成的原电池在工作过程中电流强度的变化,T时加入了H2O2 |
D.图丁表示恒温恒容条件下发生的可逆反应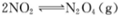 中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
已知: Cu (s)+2H+(aq)=Cu2+(aq)+ H2(g) △H 1
2H2O2(l)=2H2O(l) + O2 (g) △H 2
2H2(g) + O2(g)=2H2O(l) △H 3
则反应 Cu (s)+H2O2(l)+2H+ (aq)=Cu2+(aq)+ 2H2O(l) 的△H是
A.△H=△H 1+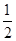 △H 2+ △H 2+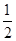 △H 3 △H 3 | B.△H=△H 1+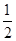 △H 2- △H 2-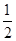 △H 3 △H 3 |
| C.△H=△H 1+2△H 2+2△H 3 | D.△H=2△H 1+△H 2+△H 3 |
已知:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol;②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol。下列结论正确的是( )
| A.碳的燃烧热大于110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
反应A(g)+B(g)―→C(g) ΔH,分两步进行:①A(g)+B(g)―→X(g) ΔH1;②X(g)―→C(g) ΔH2。反应过程中能量变化如图1所示,E1表示A+B―→X的活化能,下列说法正确的是( )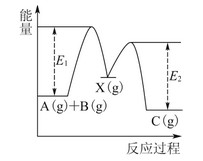
| A.ΔH1=ΔH-ΔH2>0 |
| B.X是反应A(g)+B(g)―→C(g)的催化剂 |
| C.E2是反应②的活化能 |
| D.ΔH=E1-E2 |
已知:
S(s)+O2(g) SO2(g) ΔH=-297.16 kJ·mol-1,
SO2(g) ΔH=-297.16 kJ·mol-1,
2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1。
2SO3(g) ΔH=-196.6 kJ·mol-1。
下列说法正确的是 ( )
| A.1 mol SO2(g)的能量总和大于1 mol S(s)和1 mol O2(g)的能量总和 |
| B.将2 mol SO2(g)与1 mol O2(g)在一定条件下充分反应,放出196.6 kJ的热量 |
| C.S(g)+O2(g)=SO2(g) ΔH=-Q,Q值小于297.16 kJ |
| D.当1 mol S(s)完全转化为SO3(g)时(假设无热量损失),放出395.46 kJ的热量 |
用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2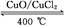 2Cl2+2H2O
2Cl2+2H2O
已知:Ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
Ⅱ.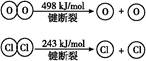
判断下列说法正确的是( )
| A.反应A的ΔH>-115.6 kJ/mol |
| B.断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为32 kJ |
| C.H2O中H—O键比HCl中H—Cl键弱 |
| D.由Ⅱ中的数据判断氯元素的非金属性比氧元素强 |
盖斯定律认为能量总是守恒的,不管化学反应过程是一步完成或分几步完成,整个过程的热效应是相同的。
已知:①H2O(g)=H2O(l) ΔH1=-Q1 kJ/mol
②C2H5OH(g)=C2H5OH(l) ΔH2=-Q2 kJ/mol
③C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)ΔH3=-Q3 kJ/mol
若使23 g液态无水酒精完全燃烧,最后恢复到室温,则放出的热量为(单位:kJ)( )
| A.Q1+Q2+Q3 | B.1.5Q1-0.5Q2+0.5Q3 |
| C.0.5Q1-1.5Q2+0.5Q3 | D.0.5(Q1+Q2+Q3) |
FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+(aq)+SCN-(aq) Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( )
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( )
| A.FeCl3(aq)与KSCN(aq)反应的热化学方程式为:Fe3+(aq)+SCN-(aq)=Fe(SCN)2+(aq) ΔH>0 |
| B.温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2 |
| C.反应处于D点时,一定有v(正)>v(逆) |
| D.A点与B点相比,A点的c(Fe3+)大 |
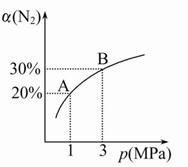
 2NH3(g)ΔH="-92.4" kJ/mol。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是( )
2NH3(g)ΔH="-92.4" kJ/mol。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是( )