已知乙炔与苯蒸气完全燃烧的热化学方程式如下所示:
①2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)
ΔH=-2 600 kJ·mol-1
②2C6H6(g)+15O2(g)=12CO2(g)+6H2O(l)
ΔH=-6 590 kJ·mol-1
下列说法正确的是( )
| A.2 mol C2H2(g)完全燃烧生成气态水时放热大于2 600 kJ |
| B.2 mol C6H6(l)完全燃烧生成液态水时放热大于6 590 kJ |
| C.相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多 |
| D.C2H2(g)三聚生成C6H6(g)的过程属于放热反应 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种反应原理如下:CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1
下列说法正确的是( )
| A.1 L CH3OH蒸汽与1 L水蒸气反应生成1 L CO2气体与3 L氢气吸收热量49.0 kJ |
| B.1个CH3OH分子与1个水分子反应生成1个CO2分子与3个H2分子吸收49.0 kJ热量 |
| C.相同条件下1 mol CH3OH(g)与1 mol H2O(g)的能量总和小于1 mol CO2(g)与3 mol H2(g)的能量总和 |
| D.1 mol CH3OH蒸汽与1 mol液态水反应生成1 mol CO2气体与3 mol氢气吸收的热量小于49.0 kJ |
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)  CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )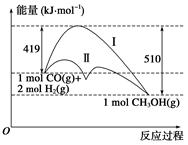
| A.该反应的ΔH=+91 kJ·mol-1 |
| B.加入催化剂,该反应的ΔH变小 |
| C.反应物的总能量大于生成物的总能量 |
| D.如果该反应生成液态CH3OH,则ΔH增大 |
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )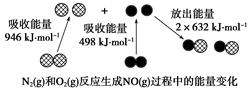
| A.1 mol N2(g)和NA个O2(g)反应放出的能量为180 kJ |
| B.1 mol N2(g)和1 mol O2(g)具有总能量小于2 mol NO(g)具有的总能量 |
| C.通常情况下,N2(g)和O2(g)混合能直接生成NO |
| D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
根据碘与氢气反应的热化学方程式
(ⅰ)I2(g)+H2(g)  2HI(g) ΔH=-9.48 kJ·mol-1
2HI(g) ΔH=-9.48 kJ·mol-1
(ⅱ)I2(s)+H2(g)  2HI(g) ΔH=+26.48 kJ·mol-1
2HI(g) ΔH=+26.48 kJ·mol-1
下列判断正确的是( )
| A.1 mol I2(s)中通入2 g H2(g),反应吸热26.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低 |
| D.反应(ⅰ)放出的热量多,所以产物的能量低,比反应(ⅱ)的产物更稳定 |
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见 ( )
| A.NH4HCO3和盐酸的反应是放热反应 |
| B.该反应中,热能转化为产物内部的能量 |
| C.反应物的总能量高于生成物的总能量 |
| D.反应的热化学方程式为NH4HCO3+HCl―→NH4Cl+CO2↑+H2O ΔH=+Q kJ·mol-1 |
已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1
③H2(g) O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
④H2O(g)=H2O(l)ΔH=-44.0 kJ·mol-1
下列结论正确的是( )
| A.碳的燃烧热大于110.5 kJ·mol-1 |
| B.浓硫酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
| C.氢气的燃烧热为241.8 kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(l)的反应热为ΔH=+571.6 kJ·mol-1 |
已知下列热化学方程式:
Na+(g)+Cl-(g)=NaCl(s) ΔH
Na(s)+ Cl2(g)=NaCl(s) ΔH1
Cl2(g)=NaCl(s) ΔH1
Na(s)=Na(g) ΔH2,Na(g)-e-=Na+(g) ΔH3 Cl2(g)=Cl(g) ΔH4,Cl(g)+e-=Cl-(g) ΔH5
Cl2(g)=Cl(g) ΔH4,Cl(g)+e-=Cl-(g) ΔH5
则ΔH与ΔH1、ΔH2、ΔH3、ΔH4、ΔH5的关系正确的是( )
| A.ΔH=ΔH1+ΔH2+ΔH3+ΔH4+ΔH5 |
| B.ΔH=ΔH1-ΔH2-ΔH3-ΔH4-ΔH5 |
| C.ΔH=ΔH1-ΔH2+ΔH3-ΔH4+ΔH5 |
| D.ΔH=ΔH2+ΔH3+ΔH4+ΔH5-ΔH1 |
向足量H2SO4溶液中加入110 mL 0.4 mol/L Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入110 mL 0.4 mol/L HCl溶液时,放出的热量是2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为( )
| A.Ba2+(aq)+SO42—(aq)=BaSO4(s)ΔH=-0.72 kJ/mol |
| B.Ba2+(aq)+SO42—(aq)=BaSO4(s)ΔH=-2.92 kJ/mol |
| C.Ba2+(aq)+SO42—(aq)=BaSO4(s)ΔH=-16.4 kJ/mol |
| D.Ba2+(aq)+SO42—(aq)=BaSO4(s)ΔH=-73.0 kJ/mol |
已知25℃时:
①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH1=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l) ΔH2=-57.3 kJ·mol-1
③Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH3<0
下列说法正确的是( )
| A.HF的电离方程式及热效应:HF(aq)=H+(aq)+F-(aq) ΔH>0 |
| B.在氢氧化钠溶液与盐酸的反应中,盐酸量一定,氢氧化钠溶液量越多,中和热越大 |
| C.ΔH2=-57.3 kJ·mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热 |
| D.稀硫酸与稀氢氧化钡溶液反应的热化学方程式为H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)ΔH=-114.6 kJ·mol-1 |