有关键能数据如表所示:
| 化学键 | N≡N | H—H | H—N |
| 键能/kJ·mol-1 | x | 436 | 391 |
A.945.6 B.649 C.431 D.869
下列有关热化学方程式或反应热的说法正确的是( )
A.已知:H2(g)+ O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则H2的燃烧热为-241.8 kJ·mol-1 O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则H2的燃烧热为-241.8 kJ·mol-1 |
| B.已知:S(g)+O2(g)=SO2(g) ΔH1=-Q1;S(s)+O2(g)=SO2(g) ΔH2=-Q2(Q1、Q2均正值),则Q1<Q2 |
C.已知: H2SO4(浓)+NaOH(aq)= H2SO4(浓)+NaOH(aq)= Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2| Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2| |
D.已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g) ΔH=+489.0 kJ·mol-1;CO(g)+ O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1;C(石墨,s)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1641 kJ·mol-1 O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1;C(石墨,s)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1641 kJ·mol-1 |
下列说法或表示方法正确的是( )
| A.反应物的总能量低于生成物的总能量时,一定不能自发进行反应 |
B.已知:CH4(g)+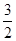 O2(g)=2H2O(l)+CO(g) ΔH,则ΔH表示CH4的燃烧热 O2(g)=2H2O(l)+CO(g) ΔH,则ΔH表示CH4的燃烧热 |
| C.恒温恒压时,将2 mol A和1 mol B投入密闭容器中,发生反应:2A(g)+B(g)??2C(g),充分反应后测得放出的热量为Q kJ,则该反应的ΔH=-Q kJ/mol |
| D.由4P(s,红磷)=P4(s,白磷) ΔH=+139.2 kJ/mol,可知红磷比白磷稳定 |
美国某技术公司开发出纳米级催化剂,可在较低温度下将甲烷转化成乙烯:2CH4(g)??C2H4(g)+2H2(g) ΔH,已知在降低温度时该反应平衡向左移动,且有下列两个反应(Q1、Q2均为正值):
反应Ⅰ:C(s)+2H2(g)=CH4(g) ΔH1=-Q1
反应Ⅱ:C(s)+H2(g)= C2H4(g) ΔH2=-Q2
C2H4(g) ΔH2=-Q2
则下列判断正确的是( )
| A.ΔH<0 | B.Q2>Q1 | C.ΔH=2(Q1-Q2) | D.ΔH=Q1-Q2 |
下列图示与对应的叙述相符的是
| A.图1表示向某硫酸和硫酸铝混合溶液中加入NaOH溶液,沉淀质量与加入NaOH溶液体积的关系 |
| B.图2表示25℃时,用0.1mol?L-1盐酸滴定20mL0.1mol?L-1NaOH溶液的pH随加入盐酸体积的变化 |
| C.图3表示t℃时稀释冰醋酸过程中溶液导电性的变化 |
| D.根据图4可判断某可逆反应的正反应是吸热反应 |
分析右图的能量变化示意图,下列选项正确的是
| A.2A+B═2C;△H>O |
| B.2C═2A+B;△H<0 |
| C.2A(g)+B(g)═2C(g)△H>0 |
| D.2A(g)+B(g)═2C(g)△H<0 |
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P—P:198,P—O:360,O=O:498,则反应P4(白磷)+3O2=P4O6的反应热ΔH为( )
| A.-1638kJ/mol | B.+1638kJ/mol |
| C.-126kJ/mol | D.+126kJ/mol |
一定量的氢气在一定条件下完全燃烧生成气态水,放出热量值为Q1,等量的H2在同样条件下完全燃烧生成液态水,放出热量值为Q2,则Q1与Q2的关系为( )
| A.Q1>Q2 | B.Q1=Q2 | C.Q1<Q2 | D.无法确定 |
下列分析正确的是( )
| A.将氯气通入H2O2和NaOH的混合溶液中,发出红光,说明反应物的总能量低于生成物的总能量,放出热量 |
| B.1mol H2在氯气中完全燃烧,放出180kJ热量,则键能(E)的关系为E(H—H)=180kJ+2E(H—Cl)-E(Cl—Cl) |
| C.干燥的碘粉与铝粉混合无明显现象,滴上一滴水会冉冉升起紫色的碘蒸气,最后得到白色AlI3。说明碘和铝发生的反应是放热反应 |
| D.精确实验测得H2O在常温下也能微弱电离:H2O??H++OH-,该过程是放热过程 |
中和热的数值是57.3kJ/mol。下列酸、碱溶液混合产生的热量等于57.3kJ的是( )
| A.1mol/L的稀HCl溶液与1mol/L的稀NaOH溶液 |
| B.1mol/L的稀H2SO4溶液与1mol/L的稀Ba(OH)2溶液 |
| C.1 L 1mol/L的稀HCl溶液与2 L 1mol/L的稀NaOH溶液 |
| D.1 L 1mol/L的稀H2SO4溶液与1 L 1mol/L的稀Ba(OH)2溶液 |