已知:N2(g)+3H2(g) ? 2 NH3(g) △H =" -92.4" kJ/mol。一定条件下,现有容积相同且恒容的密闭容器甲与乙:① 向甲中通入1 mol N2和3 mol H2,达到平衡时放出热量Q1 kJ;② 向乙中通入0.5 mol N2 和1.5 mol H2,达到平衡时放出热量Q2 kJ。则下列关系式正确的是
| A.92.4>Ql>2Q2 | B.92.4=Q1<2Q2 |
| C.Q1=2Q2=92.4 | D.Q1=2Q2<92.4 |
已知化学反应A2(g) + B2(g) = 2AB(g)的能量变化如图所示,下列叙述正确的是
| A.每生成2分子AB吸收bkJ热量 |
| B.该反应热△H=(b -a)kJ·mol-1 |
| C.反应物的总能量低于生成物的总能量 |
| D.断裂1molA—A和1molB—B键,放出akJ能量 |
下列说法不正确的是( )。
| A.化石燃料在任何条件下都能充分燃烧 |
| B.化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体 |
| C.直接燃烧煤不如将煤进行深加工后燃烧效果好 |
| D.固体煤变为气体燃料后,燃烧效率将更高 |
在反应键的H2+Cl2=2HCl中,已知H—H键的键能为436 kJ·mol-1,Cl—Cl键的键能为243 kJ·mol-1,H—Cl键的键能为431 kJ·mol-1,判断当1 mol H2与1 mol Cl2反应生成2 mol HCl时该反应( )。
| A.是吸热反应 |
| B.是放热反应 |
| C.吸收183 kJ热量 |
| D.放出183 kJ热量 |
下列反应中既属于氧化还原反应又属于放热反应的是( )。
| A.氢氧化钾与硫酸的反应 |
| B.锌与盐酸反应放出氢气 |
| C.镁条在空气中燃烧 |
| D.Ba(OH)2·8H2O与NH4Cl反应 |
吸热反应一定是( )。
| A.释放能量 |
| B.反应物总能量高于生成物总能量 |
| C.贮存能量 |
| D.反应物总能量低于生成物总能量 |
中和热测定实验中,下列操作一定会降低实验准确性的是( )
| A.用滴定管取所用药品 |
| B.NaOH溶液在倒入小烧杯时,有少量溅出 |
| C.大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多 |
| D.测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度 |
已知盐酸与硫酸跟烧碱的稀溶液反应的热化学方程式为:H+(aq)+OH-(aq) H2O(l) ΔH=Q1 kJ·mol-1,又知:H2SO4(aq)+2KOH(aq)
H2O(l) ΔH=Q1 kJ·mol-1,又知:H2SO4(aq)+2KOH(aq) K2SO4(aq)+2H2O(l)ΔH=Q2 kJ·mol-1。则Q1和Q2的关系是( )
K2SO4(aq)+2H2O(l)ΔH=Q2 kJ·mol-1。则Q1和Q2的关系是( )
| A.Q1=Q2 | B.2Q1=Q2 | C.Q1<Q2 | D.无法判断 |
将V1 mL 1.00 mol·L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2="50" mL)。下列叙述正确的是( )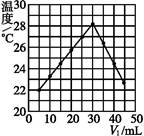
| A.做该实验时环境温度为22 ℃ |
| B.该实验表明化学能可以转化为热能 |
| C.NaOH溶液的浓度约为1.00 mol·L-1 |
| D.该实验表明有水生成的反应都是放热反应 |
已知:HCN(aq)与NaOH(aq)反应生成1 mol水的ΔH="-12.1" kJ·mol-1;HCl(aq)与NaOH(aq)反应生成1 mol水的ΔH="-57.3" kJ·mol-1。则HCN在水溶液中电离的ΔH等于( )
| A.-69.4 kJ·mol-1 | B.-45.2 kJ·mol-1 |
| C.+45.2 kJ·mol-1 | D.+69.4 kJ·mol-1 |