题目内容
下列说法不正确的是( )。
| A.化石燃料在任何条件下都能充分燃烧 |
| B.化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体 |
| C.直接燃烧煤不如将煤进行深加工后燃烧效果好 |
| D.固体煤变为气体燃料后,燃烧效率将更高 |
A
解析

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )
| A.每生成2分子AB吸收b kJ热量 |
| B.该反应热ΔH=+(a-b)kJ·mol-1 |
| C.该反应中反应物的总能量高于生成物的总能量 |
| D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量 |
在298 K、100 kPa时,已知:
2H2O(g) 2H2(g)+O2(g) ΔH1
2H2(g)+O2(g) ΔH1
Cl2(g)+H2(g) 2HCl(g) ΔH2
2HCl(g) ΔH2
2Cl2+2H2O(g) 4HCl(g)+O2(g) ΔH3
4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH2和ΔH1之间的关系正确的是( )
| A.ΔH3=ΔH1+2ΔH2 | B.ΔH3=ΔH1+ΔH2 |
| C.ΔH3=ΔH1-2ΔH2 | D.ΔH3=ΔH1-ΔH2 |
下列说法正确的是( )
| A.焓变是指1 mol物质参加反应时的能量变化 |
| B.当反应放热时ΔH>0,反应吸热时ΔH<0 |
| C.在加热条件下发生的反应均为吸热反应 |
| D.一个化学反应中,当反应物总能量大于生成物总能量时,ΔH为“-” |
已知盐酸与硫酸跟烧碱的稀溶液反应的热化学方程式为:H+(aq)+OH-(aq) H2O(l) ΔH=Q1 kJ·mol-1,又知:H2SO4(aq)+2KOH(aq)
H2O(l) ΔH=Q1 kJ·mol-1,又知:H2SO4(aq)+2KOH(aq) K2SO4(aq)+2H2O(l)ΔH=Q2 kJ·mol-1。则Q1和Q2的关系是( )
K2SO4(aq)+2H2O(l)ΔH=Q2 kJ·mol-1。则Q1和Q2的关系是( )
| A.Q1=Q2 | B.2Q1=Q2 | C.Q1<Q2 | D.无法判断 |
用H2O2和H2SO4的混合溶液可溶出废旧印刷电路板上的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+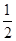 O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
在H2SO4溶液中,Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热ΔH等于( )
| A.-417.91 kJ·mol-1 | B.-319.68 kJ·mol-1 |
| C.+546.69 kJ·mol-1 | D.-448.46 kJ·mol-1 |
已知反应A+B=C+D为放热反应,对该反应的下列说法正确的是( )。
| A.A的能量一定高于C |
| B.B的能量一定高于D |
| C.A和B的总能量一定高于C和D的总能量 |
| D.该反应为放热反应,故不必加热就一定能发生 |
已知三个热化学方程式:
(1)I2(g)+H2(g)??2HI(g) ΔH=-9.48 kJ·mol-1
(2)I2(s)+H2(g)??2HI(g) ΔH=+26.48 kJ·mol-1
(3)C(石墨,s)=C(金刚石,s) ΔH>0
下列判断正确的是 ( )。
| A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(2)的反应物总能量比反应(1)的反应物总能量低 |
| D.金刚石比石墨稳定 |
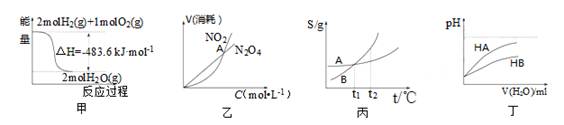
 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态