下列说法正确的是
| A.物质发生化学反应都伴随着能量变化 |
| B.伴有能量变化的物质变化都是化学变化 |
| C.在一个化学反应中,反应物的总能量与生成物的总能量一定相同 |
| D.在一个化学反应中,反应物的总能量一定高于生成物的总能量 |
已知下列热化学方程式:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g);△H="-24.8" kJ/mol
2Fe(s)+3CO2(g);△H="-24.8" kJ/mol
Fe2O3(s)+ 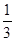 CO(g)
CO(g)
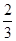 Fe3O4(s)+
Fe3O4(s)+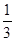 CO2(g);△H="-15.73" kJ/mol
CO2(g);△H="-15.73" kJ/mol
Fe3O4(s)+ CO(g) 3FeO(s)+CO2(g);△H="+640.4" kJ/mol
3FeO(s)+CO2(g);△H="+640.4" kJ/mol
则14 g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为 ( )
| A.-218 kJ/mol | B.-109 kJ/mol | C.+218 kJ/mol | D.+109 kJ/mol |
已知氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1 mol氢气的化学键消耗的能量为Q1 kJ,破坏1 mol氯气的化学键消耗的能量为Q2kJ ,形成1 mol氯化氢中的化学键消耗的能量为Q3kJ,下列关系式正确的是 ( )
| A.Q1 + Q2 > Q3 | B.Q1 + Q2 > 2Q3 | C.Q1 + Q2 < Q3 | D.Q1+ Q2 < 2Q3 |
分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是( )
| “嫦娥一号”发射火箭燃料 | 液氢(H2) | ①2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1 ②2H2(l)+O2(l)=2H2O(g) △H=-482.6kJ·mol-1 |
| 北京奥运会“祥云”火炬燃料 | 丙烷(C3H8) | ③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g)△H=-2013.8kJ·mol-1 ④ C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2221.5kJ·mol-1 |
C、285.8 kJ·mol-1,2013.8 kJ·mol-1 D、285.8 kJ·mol-1,2221.5 kJ·mol-1
下列说法正确的是( )
| A.需要加热才能发生的反应一定是吸热反应 |
| B.化学反应中的能量变化都表现为热量变化 |
| C.任何放热反应在常温下一定能发生反应 |
| D.反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
“摇摇冰”是一种即用即冷的饮料。吸食时将饮料罐隔离层中的化学物质和水混合后摇动即可制冷。该化学物质是 ( )
| A.氯化钠 | B.固体硝酸铵 | C.固体氢氧化钠 | D.生石灰 |
已知反应3H2+N2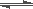 2NH3为放热反应,由此推断出 ( )
2NH3为放热反应,由此推断出 ( )
| A.氢气和氮气在常温常压下,不需要任何能量就可以迅速发生反应 |
| B.3mol氢气和1mol氮气所具有的总能量低于2mol氨气所具有的总能量 |
| C.断裂1molN≡N键和3molH—H键吸收的能量小于形成6molN—H键所放出的能量 |
| D.氢气和氮气是高能极不稳定的物质,氨气是低能且非常稳定的物质 |
下列有关说法正确的是
| A.因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差 |
| B.合成氨的反应是放热反应,则采用低温条件可以提高氨的生成速率 |
| C.常温下2S2O(g)=3S(s)+SO2(g)能自发进行,可推断该反应为放热反应 |
| D.NH4Cl和HCl溶于水后滴加石蕊都变红色,说明它们均能电离出H+ |
用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) △H=-574 kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ/mol
③H2O(g)=H2O(l) △H=-44kJ/mol。下列说法不正确的是
| A.等物质的量的CH4参加反应,反应①②转移的电子数相同 |
| B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-530 kJ/mol |
| C.0.2 mol CH4还原NO2至N2,且生成H2O(g)放出的热量为164.6 kJ |
| D.若用4.48 L(标准状况)CH4还原NO2至N2且生成H2O(g),整个过程中转移电子1.60 mol |
下列推论正确的是:
| A.S(g)+O2(g)==SO2(g)△H1;S(s)+O2(g)==SO2(g) △H2,则:△H1>△H2 |
| B.C(石墨,s)=C(金刚石,S)△H="+1.9" kJ/mol,则由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定 |
| C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(I)△H=﹣57.4 kJ/mol,则:含20 gNaOH的稀溶液与稀盐酸完全反应,放出的热量为28.7 kJ |
| D.2C(s)+O2(g)=2CO(g)△H=﹣221 kJ/mol,则碳的燃烧热等于110.5kJ/mol |