题目内容
下列有关说法正确的是
| A.因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差 |
| B.合成氨的反应是放热反应,则采用低温条件可以提高氨的生成速率 |
| C.常温下2S2O(g)=3S(s)+SO2(g)能自发进行,可推断该反应为放热反应 |
| D.NH4Cl和HCl溶于水后滴加石蕊都变红色,说明它们均能电离出H+ |
C
解析试题分析:A、有些合金抗腐蚀性能好,如不锈钢等,错误;B、低温可以提高反应物的转化率,错误;C、正确;D、前者为水解,后者为电离,错误。
考点:考查化学原理综合有关问题。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一定条件下,充分燃烧一定量的丁烷放出热量为Q kJ(Q>0),经测定完全吸收生成的二氧化碳需消耗5mol·L-1的KOH溶液100ml,恰好生成正盐,则此条件下反应: C4H10(g)+13/2O2(g)="=" 4 CO2 (g)+ 5 H2O(g)的△H为( )
| A.+8QkJ·mol-1 | B.+16Q kJ·mol-1 | C.-8Q kJ·mol-1 | D.-16Q kJ·mol-1 |
在一个容积为2 L的恒容密闭容器中加入0.2 mol CO和0.4 mol H2,发生反应:
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
实验测得在300℃和500℃时,甲醇的物质的量(mol)随时间的变化如下表所示。
| | 10 min | 20 min | 30 min | 40 min | 50 min | 60 min |
| 300℃ | 0.080 | 0.120 | 0.150 | 0.168 | 0.180 | 0.180 |
| 500℃ | 0.120 | 0.150 | 0.156 | 0.160 | 0.160 | 0.160 |
A.该反应的ΔH>0,升高温度,化学平衡常数K增大
B.300℃时,前20 min内的反应速率v(H2)="0.003" mol·L-1·min-1
C.采取加压、增大c(H2)、加入合适的催化剂等措施都能提高CO的转化率
D.500℃时,在起始时向容器中加入0.1 mol CO和0.3 mol H2,可计算出反应达平衡后甲醇的浓度
标准状态下,气态分子断开l mol化学键的焓变称为键焓。已知H-H、H-O和O-O键的键焓ΔH分别为436 kJ/mol、463 kJ/mol和495kJ/mol。下列热化学方程式正确的是
A.H2O (g)= H2(g)+ O2(g); ΔH=" -485" kJ/mol O2(g); ΔH=" -485" kJ/mol |
B.H2O (g)=H2(g)+ O2(g); ΔH="=+485" kJ/mol O2(g); ΔH="=+485" kJ/mol |
| C.2H2(g)+ O2 (g)= 2H2O(g) ΔH =" +485" kJ/mol |
| D.2H2(g)+ O 2(g)=2H2O(g) ΔH =" -485" kJ/mol |
已知氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1 mol氢气的化学键消耗的能量为Q1 kJ,破坏1 mol氯气的化学键消耗的能量为Q2kJ ,形成1 mol氯化氢中的化学键消耗的能量为Q3kJ,下列关系式正确的是 ( )
| A.Q1 + Q2 > Q3 | B.Q1 + Q2 > 2Q3 | C.Q1 + Q2 < Q3 | D.Q1+ Q2 < 2Q3 |
下列反应中,生成物的总能量大于反应物的总能量的是
| A.氢气在氧气中燃烧 | B.焦炭在高温下与水蒸气反应 |
| C.硫在氧气中燃烧 | D.铁丝在氧气中燃烧 |
下列反应前后物质的总能量变化能用下图表示的是( )
| A.生石灰和水的反应 |
| B.石灰石在高温下的分解反应 |
| C.盐酸与氢氧化钠溶液的反应 |
| D.木炭在氧气中燃烧 |
N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程中正确的是
A.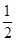 N2H4(g)+ N2H4(g)+ 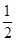 O2(g)= 1/2 N2(g)+ H2O(l)△H=+257kJ·mol-1 O2(g)= 1/2 N2(g)+ H2O(l)△H=+257kJ·mol-1 |
| B.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-133.5kJ·mol-1 |
| C.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=+534kJ·mol-1 |
| D.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ·mol-1 |
 CO2(g)+H2(g) △H<0。在850℃时,平衡常数K=1。
CO2(g)+H2(g) △H<0。在850℃时,平衡常数K=1。