下列热化学方程式中,ΔH能正确表示物质的燃烧热的是( )
| A.CO(g)+1/2O2(g)====CO2(g) ΔH=-283.0 kJ·mol-1 |
| B.C(s)+1/2O2(g)====CO(g) ΔH=-110.5 kJ·mol-1 |
| C.H2(g)+1/2O2(g)====H2O(g) ΔH=-241.8 kJ·mol-1 |
| D.2C8H18(l)+25O2(g)====16CO2(g)+18 H2O(l) ΔH=-11036 kJ·mol-1 |
以下说法正确的是( )
| A.不能自发进行的反应属于吸热反应 |
| B.化学键断裂时吸收的能量大于化学键形成时放出的能量的反应属于放热反应 |
| C.升高反应的温度,活化分子百分数增加,分子间有效碰撞的几率提高,反应速率增大 |
| D.催化剂通过改变反应路径,使反应速率增大,但不改变反应所需的活化能 |
已知化学反应2C(s)+O2(g) ="==" 2CO(g)、2CO(g)+O2(g) ===2CO2(g)都是放热反应。据此判断,下列说法不正确的是(其他条件相同)( )。
| A.12 g C所具有的能量一定高于28 g CO所具有的能量 |
| B.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量 |
| C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量 |
| D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |
如图所示,把下列物质分别加入装有水的锥形瓶里,立即塞紧带有U形管的塞子,已知U形管内预先装有少量水(为方便观察,预先将水染成红色),结果U形管左边液面升高,则加入的物质可能是( ) 
| A.NaOH固体 | B.浓硫酸 | C.NH4NO3晶体 | D.Na2O2固体 |
在298K、100kPa时,已知: ①2H2O(g)=O2(g)+2H2(g) ΔH1
② Cl2(g)+H2(g)=2HCl(g) ΔH2 ③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是
| A.Δ H3=ΔH1+2ΔH2 | B.Δ H3=ΔH1+ΔH2 |
| C.Δ H3=ΔH1-2ΔH2 | D.Δ H3=ΔH1-ΔH2 |
化学中存在一些守恒或平衡原理,下列叙述正确的是 ( )
| A.根据质量(原子)守恒定律,某物质完全燃烧的产物是CO2和H2O则该物质一定是烃 |
| B.根据能量守恒定律,所有化学反应的反应物的总能量一定等于生成物的总能量 |
| C.根据电子守恒定律,原电池中负极反应失电子数一定等于正极反应得电子数 |
| D.根据化学平衡原理,可逆反应的正反应速率在任何时刻一定等于逆反应速率 |
已知反应A+B=C+D的能量变化如图所示,下列说法正确的是 ( )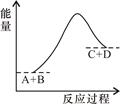
| A.该反应为放热反应 |
| B.该反应为吸热反应 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应只有在加热条件下才能进行 |
氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量。在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molF2中的化学键消耗的能量为Q2kJ,形成1molHF中的化学键释放的能量为Q3kJ。下列关系式中正确的是
| A.Q1+ Q2<2Q3 | B.Q1+ Q2>2Q3 | C.Q1+ Q2<Q3 | D.Q1+ Q2>Q3 |
下列能源中属于二次能源的是( )
| A.天然气 | B.电力 | C.原煤 | D.石油 |
 kJ,破坏1mol氯气中的化学键消耗的能量为
kJ,破坏1mol氯气中的化学键消耗的能量为 kJ,形成1mol氯化氢中的化学键释放的能量为
kJ,形成1mol氯化氢中的化学键释放的能量为 kJ。下列关系式中正确的是( )
kJ。下列关系式中正确的是( )


