��Ŀ����
��֪��ѧ��Ӧ2C(s)��O2(g) ="==" 2CO(g)��2CO(g)��O2(g) ===2CO2(g)���Ƿ��ȷ�Ӧ���ݴ��жϣ�����˵������ȷ���ǣ�����������ͬ��(����)��
| A��12 g C�����е�����һ������28 g CO�����е����� |
| B��56 g CO��32 g O2���������������88 g CO2����������� |
| C��12 g C��32 g O2���������������44 g CO2����������� |
| D����һ��������Cȼ�գ�����CO2������COʱ�ų��������� |
A
�������������A.Cȼ�ղ���CO2�����Ƿ��ȷ�Ӧ����Cȼ�ղ����IJ���CO����ų�������COȼ��Ҳ���Ƿ��ȷ�Ӧ���ɼ����ʵ�ȼ�ճ̶Ȳ�ͬ���ų��������Ͳ�ͬ������˵12 g C�����е�����һ������28 g CO�����е�����������B.����2CO(g)��O2(g) ===2CO2(g)�Ƿ��ȷ�Ӧ����56 g CO��32 g O2�����е�����������88 g CO2�����е�����������ȷ��C. 2C(s)��O2(g) ="==" 2CO(g) �Ƿ��ȷ�Ӧ, ��12 g C��32 g O2�����е�����������44 g CO2�����е�����������ȷ��D.���ڻ�ѧ��Ӧ2C(s)��O2(g) ="==" 2CO(g)��2CO(g)��O2(g) ===2CO2(g)���Ƿ��ȷ�Ӧ���ɼ������ʵ�ȼ�ճ̶Ȳ�ͬ����Ӧ�ų��������Ͳ�ͬ����ȷ��
���㣺���鷴Ӧ�������������е������Ĺ�ϵ��֪ʶ��

 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�ԭ�Ӿ���ɱ���������SiO2�ľ���ṹ�������й������ƶ��У��������
| A����������ĥ���� |
| B����������������� |
| C��������ÿ��̼ԭ���γ�2��̼��˫�� |
| D��������̼����ԭ�Ӹ���֮��Ϊ1��2 |
�״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ����
��CH3OH(g)��H2O(g)��CO2(g)��3H2(g) ?��H ����49.0 kJ/mol
��CH3OH(g)��1/2O2(g)��CO2(g)��2H2(g) ?��H����192.9 kJ/mol
����������Ӧ������˵����ȷ����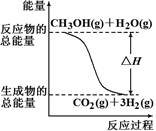
| A����Ӧ���е������仯����ͼ��ʾ |
| B������֪2H2(g)��O2(g)��2H2O(g)?��H����483.8 kJ/mol |
| C��1 mol CH3OH���ȼ�շų�������Ϊ192.9 kJ |
| D��CH3OHת���H2�Ĺ���һ��Ҫ�������� |
�����ͷ�������ںڰ������ɷ�����ը���ͷų��������������ڷ�Ӧ�����У�����1molH2�еĻ�ѧ�����ĵ�����ΪQ1kJ������1molF2�еĻ�ѧ�����ĵ�����ΪQ2kJ���γ�1molHF�еĻ�ѧ���ͷŵ�����ΪQ3kJ�����й�ϵʽ����ȷ����
| A��Q1+ Q2��2Q3 | B��Q1+ Q2��2Q3 | C��Q1+ Q2��Q3 | D��Q1+ Q2��Q3 |
̽��NaHCO3��Na2CO3������(��������Ũ�Ⱦ�Ϊ1 mol��L��1)��Ӧ�����е���ЧӦ��ʵ�����������ݣ�
| ��� | 35 mL�Լ� | ���� | ���ǰ �¶�/�� | ��Ϻ� �¶�/�� |
| �� | ˮ | 2.5 g NaHCO3 | 20.0 | 18.5 |
| �� | ˮ | 3.2 g Na2CO3 | 20.0 | 24.3 |
| �� | ���� | 2.5 g NaHCO3 | 20.0 | 16.2 |
| �� | ���� | 3.2 g Na2CO3 | 20.0 | 25.1 |
A��Na2CO3��Һ������ķ�Ӧ�����ȷ�Ӧ
B��NaHCO3��Һ������ķ�Ӧ�Ƿ��ȷ�Ӧ
C��20.0 ��ʱ����3.2 g Na2CO3�ı�����Һ��35 mL�����Ϻ���¶Ƚ�����25.1 ��
D��20.0 ��ʱ����2.5 g NaHCO3�ı�����Һ��35 mL�����Ϻ���¶Ƚ�����16.2 ��
�����Ȼ�ѧ����ʽ�У���ȷ���ǣ� ��
| A�������ȼ����Ϊ 890.3 kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ�� CH4��g��+2O2��g��=CO2��g��+2H2O(g) ��H=-890��3 kJ��mol-1 |
| B��500�桢30MPa �£��� 0��5mol N2��g���� 1��5molH2��g�������ܱ������г�ַ�Ӧ���� NH3��g������ 19��3 kJ�����Ȼ�ѧ����ʽΪ�� N2��g��+3H2��g��  2NH3��g�� ��H = -38��6 kJ��mol-1 2NH3��g�� ��H = -38��6 kJ��mol-1 |
| C��HCl �� NaOH ��Ӧ���к��ȡ�H =" -57.3" kJ��mol-1�� �� H2SO4�� Ca��OH��2��Ӧ���к��� ��H = 2����-57��3��kJ��mol -1 |
| D���� 101 kPa ʱ��2gH2��ȫȼ������Һ̬ˮ���ų� 285��8kJ ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ 2H2(g)+O2(g)=2H2O��1����H = -571��6 kJ��mol-1 |
���з�Ӧ����������ԭ��Ӧ���������ȷ�Ӧ���ǣ� ��
| A����Ƭ��ϡ���ᷴӦ | B��Ba��OH��2?8H2O��NH4Cl��Ӧ |
| C�����ȵ�̿��CO2��Ӧ | D��������O2��ȼ�� |
�ܽ���ѧ��ת��Ϊ���ܵ���
| A��������� | B��ˮ������ | C��ȼúȡů | D��ȼ�ϵ�� |
