下列说法正确的是
| A.Mg2+的半径小于N3-的半径 |
| B.H2O比H2S稳定是因为H2O中存在分子间氢键 |
| C.SiO2因的相对分子质量大于CO2,所以SiO2的熔点高于CO2 |
| D.由原子构成的晶体一定是原子晶体 |
下列各项中所描述的两个量,前者一定大于后者的是
| A.NaCl晶体和晶体NaF的晶格能 |
B.等物质的量的CO2分子和分子CH2=CH2中 键的数目 键的数目 |
| C.等物质的量的SO2和O2在一定条件下反应,SO2与O2的转化率 |
| D.25℃时pH=11的NaOH溶液和pH=11的Na2CO3溶液中的H+的浓度 |
形成物质世界多样性的原因有:( )
①元素种类 ②同位素 ③化学键成键方式 ④同分异构现象 ⑤同素异形现象
| A.仅①②③ | B.仅②④⑤ |
| C.仅①③ | D.①②③④⑤ |
下列有关比较中,大小顺序排列不正确的是( )
| A.物质的熔点:石英>食盐>冰 |
| B.热稳定性:CH4>H2S>HBr>NH3 |
| C.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| D.微粒的半径:Cl—>Na+> Mg2+> Al3+ |
硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如右图是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下面还各有一个镁原子;6个硼原子位于棱柱的侧棱上,则该化合物的化学式可表示为( )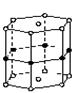
| A.MgB | B.Mg3B2 |
| C.MgB2 | D.Mg2B3 |
某化学式为AB的离子晶体,已知5r(A2+)=4r(B2-)(各类离子晶体与 关系如下图所示),经测定其密度为
关系如下图所示),经测定其密度为 g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
| r+/r- | 配位数 | 实例 |
| 0.225~0.414 | 4 | ZnS |
| 0.414~0.732 | 6 | NaCl |
| 0.732~1.0 | 8 | CsCl |
| >1.0 | 12 | CsF |
A.该晶体结构与ZnS晶体相似
B.该晶体每个晶胞中有2个A2+和B2-
C.该晶体晶胞的边长为
 cm
cmD.A2+离子紧邻的B2-构成的空间结构为立方体
表中原子化热、晶格能、键能的单位都是kJ·mol-1
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
则下列说法正确的是( )
A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ
B.Si(s)+2Cl2(g)=SiCl4(g) △H=-602kJ·mol-1
C.从表中可以看出,氯化钠的熔点比晶体硅高
D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强
下面有关晶体的叙述中,错误的是( )
| A.金刚石网状结构中,碳原子和共价键的个数比为1:2 |
| B.氯化钠晶体中,每个Na+周围距离相等的Cl-肯定为6个 |
| C.氯化铯晶体中,每个Cs+周围紧邻6个Cs+ |
| D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |

 键
键