最近科学家成功地制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是( )。
| A.该物质的化学式为CO4 |
| B.晶体的熔、沸点高,硬度大 |
| C.晶体中C原子数与C—O键数之比为1∶4 |
| D.晶体的空间最小环共由12个原子所构成 |
纳米材料是21世纪最有前途的新型材料之一,世界各国对这一新材料给予了极大的关注。纳米粒子是指直径为1~100 nm的超细粒子(1 nm=10-9 m)。由于表面效应和体积效应,其常有奇特的光、电、磁、热等性能,可开发为新型功能材料,有关纳米粒子的叙述不正确的是( )。
| A.因纳米粒子半径太小,故不能将其制成胶体 |
| B.一定条件下纳米粒子可催化水的分解 |
| C.一定条件下,纳米陶瓷可发生任意弯曲,可塑性好 |
| D.纳米粒子半径小,表面活性高 |
电子表、电子计算器、电脑显示器都运用了液晶材料显示图像和文字。有关其显示原理的叙述中,正确的是 ( )。
| A.施加电场时,液晶分子沿垂直于电场方向排列 |
| B.移去电场后,液晶分子恢复到原来状态 |
| C.施加电场后,液晶分子恢复到原来状态 |
| D.移去电场后,液晶分子沿电场方向排列 |
下列数据对应物质的熔点,据此作出下列判断中错误的是( )。
| Na2O | NaCl | AlF3 | AlCl3 |
| 920 ℃ | 801 ℃ | 1 292 ℃ | 190 ℃ |
| BCl3 | Al2O3 | CO2 | SiO2 |
| -107 ℃ | 2 073 ℃ | -57 ℃ | 1 723 ℃ |
A.铝的化合物的晶体中有离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
下列说法中正确的是(NA为阿伏加德罗常数)( )
| A.28 g晶体硅中含有Si—Si键的个数为2NA |
| B.124 g白磷(P4)晶体中含有P—P键的个数为4NA |
| C.12 g金刚石中含有C—C键的个数为4NA |
| D.SiO2晶体中每1 mol Si可与氧原子形成2NA个共价键(Si—O键) |
在下列四种有关性质的叙述中,可能属于金属晶体的是( )
| A.由分子间作用力结合而成,熔点低 |
| B.固体或熔融后易导电,熔点在1000℃左右 |
| C.由共价键结合成网状结构,熔点高 |
| D.固体不导电,但溶于水或熔融后能导电 |
干燥剂的干燥性能可用干燥效率(1m3空气中实际余留水蒸气的质量)来衡量。某些干燥剂的干燥效率数据如下:
| 物质 | 干燥效率 | 物质 | 干燥效率 |
| MgO | 0.008 | ZnCl2 | 0.8 |
| CaO | 0.2 | ZnBr2 | 1.1 |
分析以上数据,下列有关叙述错误的是
A.MgO的干燥性能比CaO好
B.干燥效率可能与干燥剂的阴、阳离子的半径大小有关
C.MgCl2可能是比CaCl2更好的干燥剂
D.上述干燥剂中阳离子对干燥性能的影响比阴离子小
类推是化学学习和研究中常用的思维方法.下列类推错误的是
①Mg可由电解熔融MgCl2制取;则Al也可由电解熔融AlCl3制取
②晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子
③1mol/L的NaCl溶液每升中含有1mol Na+;则1mol/L的FeCl3溶液每升中也含有1molFe3+
④使用pH试纸时必须保持干燥,则湿润的pH试纸测得的pH一定有误差
| A.①③ | B.①③④ | C.②③④ | D.①②③④ |
有关晶体的结构如图所示,下列说法中不正确的是( )。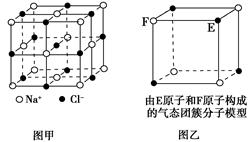
| A.在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体 |
| B.该气态团簇分子(图乙)的分子式为EF或FE |
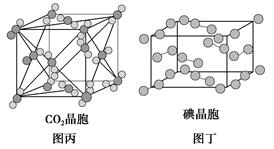
| C.在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻 |
| D.在碘晶体(图丁)中,碘分子的排列有两种不同的方向 |
